Формула безводной уксусной кислоты. Химия: Уксусная кислота, Реферат
на тему:
Выполнил:_____________
______________________
Проверил:_____________
______________________
Волгоград 2004
Введение………………………………………………….3
1. Открытие уксусной кислоты……………………..5
2. Свойства уксусной кислоты……………………..13
3. Получение уксусной кислоты……………………19
4. Применение уксусной кислоты………………….22
Заключение……………………………………………....26
Список использованной литературы………………..…27
Введение
УКСУСНАЯ КИСЛОТА, CH3COOH, бесцветная горючая жидкость с резким запахом, хорошо растворимая в воде. Имеет характерный кислый вкус, проводит электрический ток.
Уксусная кислота была единственной, которую знали древние греки. Отсюда и ее название: "оксос" - кислое, кислый вкус. Уксусная кислота - это простейший вид органических кислот, которые являются неотъемлемой частью растительных и животных жиров. В небольших концентрациях она присутствует в продуктах питания и напитках и участвует в метаболических процессах при созревании фруктов. Уксусная кислота часто встречается в растениях, в выделениях животных. Соли и эфиры уксусной кислоты называются ацетатами.
Уксусная кислота - слабая (диссоциирует в водном растворе только частично). Тем не менее, поскольку кислотная среда подавляет жизнедеятельность микроорганизмов, уксусную кислоту используют при консервировании пищевых продуктов, например, в составе маринадов.
Получают уксусную кислоту окислением ацетальдегида и другими методами, пищевую уксусную кислоту уксуснокислым брожением этанола. Применяют для получения лекарственных и душистых веществ, как растворитель (например, в производстве ацетата целлюлозы), в виде столового уксуса при изготовлении приправ, маринадов, консервов. Уксусная кислота участвует во многих процессах обмена веществ в живых организмах. Это одна из летучих кислот, присутствующая почти во всех продуктах питания, кислая на вкус и главная составляющая уксуса.
Цель данной работы: изучить свойства, производство и применение уксусной кислоты.
Задачи данного исследования:
1. Рассказать об истории открытия уксусной кислоты
2. Изучить свойства уксусной кислоты
3. Описать способы получения уксусной кислоты
4. Раскрыть особенности применения уксусной кислоты
1. Открытие уксусной кислоты
Строение уксусной кислоты заинтересовало химиков со времени открытия Дюма трихлоруксусной кислоты, так как этим открытием был нанесен удар господствовавшей тогда электрохимической теории Берцелиуса. Последний, распределяя элементы на электроположительные и электроотрицательные, не признавал возможности замещения в органических веществах, без глубокого изменения их химических свойств, водорода (элемента электроположительного) хлором (элементом электроотрицательным), а между тем по наблюдениям Дюма ("Comptes rendus" Парижской академии, 1839) оказалось, что "введение хлора на место водорода не изменяет совершенно внешних свойств молекулы...", почему Дюма и задается вопросом "покоятся ли электрохимические воззрения и представления о полярности, приписываемой молекулам (атомам) простых тел, на столь ясных фактах, чтобы их можно было считать предметами безусловной веры; если же их должно рассматривать как гипотезы, то подходят ли эти гипотезы к фактам?... Должно признать, продолжает он, что дело обстоит иначе. В неорганической химии путеводной нитью нам служит изоморфизм, теория, основанная на фактах, как хорошо известно, мало согласных с электрохимическими теориями. В органической химии ту же роль играет теория замещения... и может быть будущее покажет, что оба воззрения более тесно связаны между собою, что они вытекают из одних и тех же причин и могут быть обобщены под одним и тем же названием. Пока же на основании превращения У. кислоты в хлоруксусную и альдегида в хлоральдегид (хлорал) и из того обстоятельства, что в этих случаях весь водород может быть замещен равным ему объемом хлора без изменения основного химического характера вещества, можно вывести заключение, что в органической химии существуют типы, которые сохраняются и тогда, когда на место водорода мы вводим равные объемы хлора, брома и йода. А это значит, что теория замещения покоится на фактах и при том наиболее блестящих в органической химии". Приводя эту выдержку в своем годовом отчете шведской академии ("Jahresbericht etc.", т. 19, 1840, стр. 370). Берцелиус замечает: "Дюма приготовил соединение, которому он придает рациональную формулу C4Cl6O3+H2O (Атомные веса современные; трихлоруксусная кислота рассматривается, как соединение ангидрида с водою.); это наблюдение он причисляет к faits les plus eclatants de la Chimie organique; это - основание его теории замещения. которая, по его мнению, опрокинет электрохимические теории..., а между тем оказывается, что стоит только его формулу написать несколько иначе, чтобы иметь соединение щавелевой кисл. с соответственным хлоридом, C2Cl6+C2O4H2, который остается соединенным со щавелевой кислотою и в кислоте, и в солях. Мы, следовательно, имеем дело с таким родом соединения, примеров которого известно много; многие... как простые, так и сложные радикалы обладают тем свойством, что их кислородсодержащая часть может вступать в соединение с основаниями и их лишаться, не теряя связи с хлорсодержащей частью. Это воззрение не приведено Дюма и не подвергнуто им опытной проверке, а между тем, если оно верно, то у нового учения, несовместимого, по Дюма, с господствовавшими до сих пор теоретическими представлениями, вырвана из под ног почва и оно должно пасть". Перечислив затем некоторые неорганические соединения, подобные, по его мнению, хлоруксусной кислоте (Между ними Берцелиусом приведен и хлор ангидрид хромовой кислоты - CrO2Cl2, который он считал за соединение надхлорного хрома (неизвестного и по сие время) с хромовым ангидридом: 3CrO2Cl2=CrCl6+2CrO3), Берцелиус продолжает: "хлоруксусная кислота Дюма, очевидно, принадлежит к этому классу соединений; в ней радикал углерода соединен и с кислородом, и с хлором. Она может быть, следовательно, щавелевой кислотою, в которой половина кислорода замещена хлором, или же соединением 1 атома (молекулы) щавелевой кислоты с 1 атомом (молекулой) полуторохлористого углерода - C2Cl6. Первое предположение не может быть принято, потому что оно допускает возможность замещения хлором 11/2, атомов кислорода (По Берцелиусу щавелевая кислота была C2O3.). Дюма же держится третьего представления, совершенно несовместимого с двумя вышеизложенными, по которому хлор замещает не кислород, а электроположительный водород, образуя углеводород C4Cl6, обладающий теми же свойствами сложного радикала, как и C4H6 или ацетил, и способный якобы с 3 атомами кислорода давать кислоту, тожественную по свойствам с У., но, как видно из сравнения (их физических свойств), вполне от нее отличную". Насколько Берцелиус в то время был глубоко убежден в различной конституции уксусной и трихлоруксусной кислоты, видно хорошо из замечания, высказанного им в том же году ("Jahresb.", 19, 1840, 558) по поводу статьи Жерара ("Journ. f. pr. Ch.", XIV, 17): "Жерар, говорит он, высказал новый взгляд на состав спирта, эфира и их производных; он следующий: известное соединение хрома, кислорода и хлора имеет формулу = CrO2Cl2, хлор замещает в нем атом кислорода (Подразумевается Берцелиусом 1 атом кислорода хромового ангидрида - CrO3). У. кислота C4H6+3O заключает в себе 2 атома (молекулы) щавелевой кислоты, из которых в одном весь кислород замещен водородом = C2O3+C2H6. И такой игрой в формулы заполнены 37 страниц. Но уже в следующем году Дюма, развивая далее идею типов, указал, что, говоря о тожестве свойств У. и трихлоруксусной кислоты, он подразумевал тожество их химических свойств, наглядно выражающееся, напр., в аналогии распадения их под влиянием щелочей: C2H3O2K + KOH = CH4 + K2CO8 и С2Cl3O2K + KOH = CHCl3 + K2CO8, так как CH4 и CHCl3 являются представителями одного и того же механического типа. С другой стороны, Либих и Греэм публично высказались за большую простоту, достигаемую на почве теории замещения, при рассмотрении хлоропроизводных обыкновенного эфира и эфиров муравьиной и У. кисл., полученных Малагутти, и Берцелиус, уступая давлению новых фактов, в 5-м изд. своего "Lehrbuch der Chemie" (Предисловие помечено ноябрем 1842 г.), позабыв свой резкий отзыв о Жераре, нашел возможным написать следующее: "Если мы припомним превращение (в тексте разложение) уксусной кислоты под влиянием хлора в хлорощавелевую кислоту (Хлорощавелевой - Chloroxalsaure - Берцелиус называет трихлоруксусную кисл. ("Lehrbuch", 5 изд., стр. 629).), то представляется возможным еще другой взгляд на состав уксусной кислоты (уксусная кислота называется Берцелиусом Acetylsaure.), а именно - она может быть сочетанной щавелевой кислотой, в которой сочетающейся группой (Paarling) является C2H6, подобно тому, как сочетающейся группой в хлорощавелевой кислоте является C2Cl6, и тогда действие хлора на уксусную кислоту состояло бы только в превращении C2H6 в C2Cl6. Понятно, нельзя решить, является ли такое представление более правильным..., однако, полезно обратить внимание на возможность его".
Таким образом, Берцелиусу пришлось допустить возможность замещения водорода хлором без изменения химической функции первоначального тела, в котором происходить замещение. Не останавливаясь на приложении его воззрений к другим соединениям, перехожу к работам Кольбе, который для уксусной кислоты, а затем и для других предельных одноосновных кислот нашел ряд фактов, гармонировавших со взглядами Берцелиуса (Жерара). Исходной точкой для работ Кольбе послужило изучение кристаллического вещества, состава CCl4SO2, полученного ранее Берцелиусом и Марсэ при действии царской водки на CS2 и образовавшегося у Кольбе при действии на CS2 влажного хлора. Рядом превращений Кольбе (См. Kolbe, "Beitrage znr Kenntniss der gepaarten Verbindungen" ("Ann. Ch. u. Ph.", 54, 1845, 145).) показал, что это тело представляет, выражаясь современным языком, хлор ангидрид трихлорометилсульфоновой кислоты, CCl4SO2 = CCl3.SO2Cl (Кольбе его назвал Schwefligsaures Kohlensuperchlorid), способный под влиянием щелочей давать соли соответственной кислоты - CCl3.SO2(OH) [по Кольбе НО + C2Cl3S2O5 - Chlorkohlenunterschwefelsaure] (Атомные веса: H=2, Cl=71, С=12 и О=16; а потому при современных атомных весах она - С4Сl6S2O6H2.) , которая под влиянием цинка замещает сначала один атом Сl водородом, образуя кислоту CHCl2.SO2(OH) [по Кольбе - wasserhaltige Chlorformylunterschwefelsaure (Берцелиус ("Jahresb. " 25, 1846, 91) замечает, что правильные считать ее сочетанием дитионовой кислоты S2O5 с хлороформилом, почему он CCl3SO2(OH) называет Kohlensuperchlorur (C2Cl6) - Dithionsaure (S2O5). Гидратная вода, по обыкновению, Берцелиусом не принимается во внимание.), а затем и другой, образуя кислоту CH2Cl.SO2(OH) [по Кольбе - Chlorelaylunterschwefelsaure], а, наконец, при восстановлении током или калиевой амальгамой (Реакция незадолго перед тем была применена Мельсансом для восстановления трихлоруксусной кислоты в уксусную.) замещает водородом и все три атома Сl, образуя метилсульфоновую кисл. CH3.SO2(OH) [по Кольбе - Methylunterschwefelsaure]. Аналогия этих соединений с хлороуксусными кислотами невольно бросалась в глаза; действительно, при тогдашних формулах получались два параллельных ряда, как видно из следующей таблички: H2O+C2Cl6.S2O5 H2O+C2Cl6.C2O3 H2O+C2H2Cl4.S2O5 H2O+C2H2Cl4.C2O3 H2O+C2H4Cl2.S2O5 H2O+C2H4Cl2.C2O3 H2O+C2H6.S2O5 H2O+C2H6.C2O3 Это и не ускользнуло от Кольбе, который замечает (I. с. стр. 181): "к описанным выше сочетанным сернистым кислотам и непосредственно в хлороуглеродсернистой кислоте (выше - H2O+C2Cl6.S2O5) примыкает хлорощавелевая кислота, известная еще под названием хлоруксусной кислоты. Жидкий хлороуглерод - ССl (Сl=71, С=12; теперь мы пишем C2Cl4 - это хлороэтилен.), как известно, превращается на свету под влиянием хлора в - гексахлорэтан (по тогдашней номенклатуре - Kohlensuperchlorur), и можно ожидать, что, если бы его одновременно подвергнуть действию воды, то он, подобно хлористому висмуту, хлорной сурьме и т. д., в момент образования, заместит хлор кислородом. Опыт подтвердил предположение". При действии света и хлора на C2Cl4, находившийся под водою, Кольбе получил на ряду с гексахлорэтаном и трихлоруксусную кислоту и выразил превращение таким уравнением: (Так как С2Сl4 может быть получен из CCl4 при пропускании его через накаленную) трубку, а ССl4 образуется при действии, при нагревании, Cl2 на CS2 то реакция Кольбе была первым по времени синтезом уксусной кислоты из элементов.) "Образуется ли одновременно и свободная щавелевая кисл., трудно решить, так как на свету хлор тотчас же окисляет ее в уксусную кислоту"... Воззрение Берцелиуса на хлоруксусную кислоту "удивительным образом (auf eine tiberraschende Weise) подтверждается существованием и параллелизмом свойств сочетанных сернистых кислот, и, как мне кажется (говорит Кольбе I. с. стр. 186), выходит из области гипотез и приобретает высокую степень вероятности. Ибо, если хлороуглещавелевая (Chlorkohlenoxalsaure так теперь Кольбе называет хлоруксусную кислоту.) имеет состав, подобный составу хлороуглесернистой кислоты, то мы должны считать и уксусную кислоту, отвечающую метилсернистой, за сочетанную кислоту и рассматривать ее, как метилщавелевую: C2H6.C2O3 (Это взгляд, высказанный ранее Жераром). Не невероятно, что мы будем принуждены в будущем принять за сочетанные кислоты значительное число тех органических кислот, в которых в настоящее время, в силу ограниченности наших сведений - мы принимаем гипотетическиe радикалы... " "Что касается явлений замещения в этих сочетанных кислот, то они получают простое объяснение в том обстоятельстве, что различные, вероятно, изоморфные соединения способны замещать друг друга в роли сочетающихся групп (als Раarlinge, l. с. стр. 187), не изменяя существенно кислых свойств сочетанного с ними тела!" Дальнейшее экспериментальное подтверждение этого взгляда мы находим в статье Франкланда и Кольбе: "Ueber die chemische Constitution der Sauren der Reihe (CH2)2nO4 und der unter den Namen "Nitrile" bekannten Verbindungen" ("Ann. Chem. n. Pharm. ", 65, 1848, 288). Исходя из представления, что все кислоты ряда (CH2)2nO4, построены подобно метилщавелевой кислоте (Теперь мы пишем CnH2nO2 и называем метилщавелевую кислоту - уксусной.), они замечают следующее: "если формула H2O+H2.C2O3 представляет истинное выражение рационального состава муравьиной кислоты, т. е. если ее считать за щавелевую кислоту, сочетанную с одним эквивалентом водорода (Выражение не верно; вместо Н гг. Франкланд и Кольбе употребляют перечеркнутую букву, которая равноценна 2 Н.), то без труда объясняется превращение при высокой температуре муравьинокислого аммония в водную синильную кислоту, потому что известно, и найдено еще Доберейнером, что щавелевокислый аммоний распадается при нагревании на воду и циан. Сочетанный в муравьиной кислоте водород участвует в реакции только тем, что он, соединяясь с цианом, образует синильную кислоту: Обратное образование муравьиной кислоты из синильной под влиянием щелочей представляет не что иное, как повторение известного превращения растворенного в воде циана в щавелевую кислоту и аммиак, с тою лишь разницей; что в момент образования щавелевая кислота сочетается с водородом синильной кислоты". То, что цианистый бензол (С6H5CN), например, по Фелингу, не обладает кислыми свойствами и не образует берлинской лазури может быть, по мнению Кольбе и Франкланда, поставлено в параллель с неспособностью хлора хлористого этила к реакции с AgNO3, и правильность их наведения Кольбе и Франкланд доказывают синтезом по методу нитрилов (Нитрилы ими получались перегонкой серновинных кислот с KCN (методом Дюма и Малагутти с Лебланом): R".SO3(OH)+KCN=R.CN+KHSO4) уксусной, пропионовой (по тогдашнему, мет-ацетоновой,) и капроновой кислоты, Затем, в следующем году Кольбе подверг электролизу щелочные соли одноосновных предельных кислот и, в согласии со своей схемой, наблюдал при этом, при электролизе уксусной кислоты, образование этана, угольной кислоты и водорода: H2O+C2H6.C2O3=H2+, а при электролизе валериановой - октана, угольной же кислоты и водорода: H2O+C8H18.C2O3=H2+ . Впрочем, нельзя не заметить, что Кольбе ожидал получить из уксусной кислоты метил (СН3)", соединенный с водородом, т. е. болотный газ, а из валериановой - бутил C4H9 , тоже соединенный с водородом, т. е. C4H10 (он называет C4H9 валлилом), но в этом ожидании надо видеть уступку получившим уже тогда значительные права гражданства формулам Жерара, который отказался от своего прежнего взгляда на уксусную кислоту и считал ее не за C4H8O4 каковой формулой, судя по криоскопическим данным, она обладает и на самом деле, а за C2H4O2 , как пишется во всех современных учебниках химии.
Работами Кольбе строение уксусной кислоты, а вместе с тем и всех других органических кислот было окончательно выяснено и роль последующих химиков свелась только к делению - в силу теоретических соображений и авторитета Жерара, формул Кольбе пополам и к переведению их на язык структурных воззрений, благодаря чему формула C2H6.C2O4H2 превратилась в CH3.CO(OH).
2. Свойства уксусной кислоты
Карбоновые кислоты - органические соединения, содержащие одну или несколько карбоксильных групп –СООН, связанных с углеводородным радикалом.
Кислотные свойства карбоновых кислот обусловлены смещением электронной плотности к карбонильному кислороду и вызванной этим дополнительной (по сравнению со спиртами) поляризации связи О–Н.
В водном растворе карбоновые кислоты диссоциируют на ионы:
С увеличением молекулярной массы растворимость кислот в воде уменьшается.
По числу карбоксильных групп кислоты подразделяются на одноосновные (монокарбоновые) и многоосновные (дикарбоновые, трикарбоновые и т.д.).
По характеру углеводородного радикала различают кислоты предельные, непредельные и ароматические .
Систематические названия кислот даются по названию соответствующего углеводорода с добавлением суффикса -овая и слова кислота . Часто используются также тривиальные названия.
Некоторые предельные одноосновные кислоты
| Формула | Название |
|
| систематическое | тривиальное |
|
| HCOOH | метановая | муравьиная |
| этановая | уксусная | |
| пропановая | пропионовая | |
| бутановая | масляная | |
| пентановая | валерьяновая | |
| гексановая | капроновая | |
| пентадекановая | пальмитиновая | |
| гептадеканова | стеариновая | |
Карбоновые кислоты проявляют высокую реакционную способность. Они вступают в реакции с различными веществами и образуют разнообразные соединения, среди которых большое значение имеют функциональные производные , т.е. соединения, полученные в результате реакций по карбоксильной группе .
2.1 Образование солей
а) при взаимодействии с металлами:
2RCOOH + Mg ® (RCOO) 2 Mg + H 2
б) в реакциях с гидроксидами металлов:
2RCOOH + NaOH ® RCOONa + H 2 O
Вместо карбоновых кислот чаще используют их галогенангидриды:
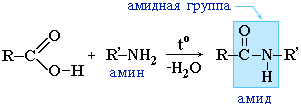 |
Амиды образуются также при взаимодействии карбоновых кислот (их галогенангидридов или ангидридов) с органическими производными аммиака (аминами):
Амиды играют важную роль в природе. Молекулы природных пептидов и белков построены из a-аминокислот с участием амидных групп - пептидных связей.
Уксусная (этановая кислота).
Формула: СН 3 – СООН; прозрачная бесцветная жидкость с резким запахом; ниже температуры плавления (т.пл. 16,6 градусов С) похожая на лед масса (поэтому концентрированную уксусную кислоту называют также ледяной уксусной кислотой). Растворима в воде, этаноле .
Таблица 1. Физические свойства уксусной кислоты
| Название | Формула | tкип. | Раство- | Ka |
||||
| кислоты | её соли |
|||||||
| уксусная | этановая | ацетат | CH3COOH | 16,8 | 118 | 1,05 | ¥ | 1,7.10-5 |
Синтетическая пищевая уксусная кислота – бесцветная, прозрачная, легковоспламеняющаяся жидкость с резким запахом уксуса. Синтетическую пищевую уксусную кислоту получают из метанола и окиси углерода на родиевом катализаторе. Синтетическая пищевая уксусная кислота применяется в химической, фармацевтической и легкой промышленности, а также в пищевой промышленности в качестве консерванта. Формула СН 3 СООН.
Синтетическая пищевая уксусная кислота выпускается концентрированной (99.7 %) и в виде водного раствора (80 %).
По физико-химическим показателям синтетическая пищевая уксусная кислота должна соответствовать следующим нормам:
Таблица 2. Основные технические требования
| Наименование показателя | |
| 1. Внешний вид | Бесцветная, прозрачная жидкость без механических примесей |
| 2. Растворимость в воде | Полная, раствор прозрачный |
| 3. Массовая доля уксусной кислоты, %, не менее | 99,5 |
| 4. Массовая доля уксусного альдегида, %, не более | 0,004 |
| 5. Массовая доля муравьиной кислоты, %, не более | 0,05 |
| 6. Массовая доля сульфатов (SO 4), %, не более | 0,0003 |
| 7. Массовая доля хлоридов (Cl),%, не более | 0,0004 |
| 8. Массовая доля тяжелых металлов осаждаемых сероводородом (Pb), %, не более | 0,0004 |
| 9. Массовая доля железа (Fe), %, не более | 0,0004 |
| 10. Массовая доля нелетучего остатка, %, не более | 0,004 |
| 11. Устойчивость окраски раствора марганцевокислого калия, мин, не менее | 60 |
| 12. Массовая доля веществ, окисляемых двухромовокислым калием, cm 3 раствора тиосульфата натрия, концентрация с (Na 2 SO 3 *5H 2 O) = 0,1 моль/дм 3 (0,1H), не более | 5,0 |
Синтетическая пищевая уксусная кислота – легковоспламеняющаяся жидкость, по степени воздействия на организм относится к веществам 3-го класса опасности. При работе с уксусной кислотой следует применять индивидуальные средства защиты (фильтрующие противогазы). Первая помощь при ожогах - обильное промывание водой.
Синтетическую пищевую уксусную кислоту заливают в чистые железнодорожные цистерны, автоцистерны с внутренней поверхностью из нержавеющей стали, в контейнеры, емкости и бочки из нержавеющей стали вместимостью до 275 дм3, а также в стеклянные бутыли и полиэтиленовые бочки вместимостью до 50 дм3. Полимерная тара пригодна для залива и хранения уксусной кислоты в течение одного месяца. Синтетическую пищевую уксусную кислоту хранят в герметичных резервуарах из нержавеющей стали. Контейнеры, емкости, бочки, бутыли и полиэтиленовые фляги хранят в складских помещениях или под навесом. Не допускается совместное хранение с сильными окислителями (азотная кислота, серная кислота, перманганат калия и др.).
Транспортируется в ж/д цистернах, изготовленных из нержавеющей стали марки 12Х18H10Т или 10Х17H13М2Т, с верхним сливом.
3. Получение уксусной кислоты
Уксусная кислота - важнейший химический продукт, который широко используется в промышленности для получения сложных эфиров, мономеров (винилацетат), в пищевой промышленности и т.д. Мировое производство ее достигает 5 млн т в год. Получение уксусной кислоты до недавнего времени базировалось на нефтехимическом сырье . В Уокер-процессе этилен в мягких условиях окисляют кислородом воздуха до ацетальдегида в присутствии каталитической системы PdCl2 и CuCl2 . Далее ацетальдегид окисляется до уксусной кислоты:
CH2=CH2 + 1/2 O2 CH3CHO CH3COOH
По другому методу уксусную кислоту получают при окислении н-бутана при температуре 200 C и давлении 50 атм в присутствии кобальтового катализатора.
Изящный Уокер-процесс - один из символов развития нефтехимии - постепенно замещается новыми методами, основанными на использовании угольного сырья. Разработаны способы получения уксусной кислоты из метанола:
CH3OH + CO CH3COOH
Эта реакция, имеющая большое промышленное значение, является прекрасным примером, иллюстрирующим успехи гомогенного катализа. Поскольку оба компонента реакции - СН3ОН и СО - могут быть получены из угля, процесс карбонилирования должен стать более экономичным по мере роста цен на нефть. Существуют два промышленных процесса карбонилирования метанола. В более старом методе, разработанном на фирме BASF, использовали кобальтовый катализатор, условия реакции были жесткими: температура 250?С и давление 500-700 атм. В другом процессе, освоенном фирмой "Monsanto", применяли родиевый катализатор, реакцию проводили при более низких температурах (150-200 С) и давлении (1-40 атм). Интересна история открытия этого процесса. Ученые компании исследовали гидроформилирование с использованием родийфосфиновых катализаторов. Технический директор нефтехимического отдела предложил использовать этот же катализатор для карбонилирования метанола. Результаты опытов оказались отрицательными, и это связали с трудностью образования связи металл-углерод. Однако, вспомнив лекцию консультанта компании о легком окислительном присоединении иодистого метила к металлокомплексам, исследователи решили добавить в реакционную смесь иодный промотор и получили блестящий результат, которому сперва не поверили. Подобное открытие было сделано также учеными конкурирующей компании "Union Carbide", те отстали всего на несколько месяцев. Команда по разработке технологии карбонилирования метанола всего через 5 месяцев интенсивной работы создала промышленный процесс Монсанто, с помощью которого в 1970 году было получено 150 тыс. т уксусной кислоты. Этот процесс стал предвестником той области науки, которая получила название С1-химии.
Механизм карбонилирования был тщательно исследован. Иодистый метил, необходимый для осуществления реакции, получается по уравнению
CH3OH + HI CH3I + H2O
Каталитический цикл может быть представлен так:
К плоскоквадратному комплексу - (I) окислительно присоединяется иодистый метил с образованием шестикоординационного комплекса II, затем в результате внедрения СО по связи метил-родий образуется ацетилродиевый комплекс (III). Восстановительное элиминирование иодангидрида уксусной кислоты регенерирует катализатор, а гидролиз иодангидрида дает уксусную кислоту.
Промышленный синтез уксусной кислоты:
a) каталитическое окисление бутана
2CH3–CH2–CH2–CH3 + 5O2 t 4CH3COOH + 2H2O
b) нагреванием смеси оксида углерода (II) и метанола на катализаторе под давлением
CH3OH + CO CH3COOH
Производство уксусной кислоты брожением (уксуснокислое брожение) .
Сырье: этанолсожержащие жидкости (вино, забродившие соки), кислород.
Вспомогательные вещества: ферменты уксуснокислых бактерий.
Химическая реакция: этанол биокаталитически окисляется до уксусной кислоты.
СН 2 – СН – ОН + О 2 СН 2 – СООН + Н 2 О
Основной продукт: уксусная кислота.
4. Применение уксусной кислоты
Уксусную кислоту применяют для получения лекарственных и душистых веществ, как растворитель (например, в производстве ацетата целлюлозы), в виде столового уксуса при изготовлении приправ, маринадов, консервов.
Водный раствор уксусной кислоты используют в качестве вкусового и консервирующего средства (приправа к пище, маринование грибов, овощей).
В состав уксуса входят такие кислоты, как яблочная, молочная, аскорбиновая, уксусная.
Яблочный уксус(4% уксусной кислоты)
Яблочный уксус содержит 20 важнейших минеральных веществ и микроэлементов, а также уксусную, пропионовую, молочную и лимонную кислоты, целый ряд ферментов и аминокислот, ценные балластные вещества, такие, как поташ, пектин. Яблочный уксус широко применяется при приготовлении различных блюд и консервировании. Он прекрасно сочетается со всевозможными салатами, как из свежих овощей, так и мясными и рыбными. В нем можно мариновать мясо, огурцы, капусту, каперсы, портулак, а также трюфели. Однако, на Западе яблочный уксус известен больше своими лечебными свойствами. Он применяется при повышенном кровяном давлении, мигренях, астме, головной боли, алкоголизме, головокружении, артрите, болезнях почек, высокой температуре, ожогах, пролежнях и др.
Здоровым людям рекомендуется каждый день употреблять полезный и освежающий напиток: в стакане воды размешать ложку меда и добавить 1 ложку яблочного уксуса. Желающим похудеть, рекомендуем каждый раз во время еды выпивать стакан несладкой воды с двумя ложками яблочного уксуса.
Уксус широко используется в домашнем консервировании для приготовления маринадов различной крепости. В народной медицине уксус используется как неспецифическое жаропонижающее средство (путем протирания кожи раствором воды и уксуса в пропорции 3:1), а также при головных болях методом примочек. Распространено применение уксуса при укусах насекомых посредством компрессов.
Известно применение спиртового уксуса в косметологии. А именно для придания мягкости и блеска волосам после химической завивки и перманентной окраски. Для этого волосы рекомендуется ополаскивать теплой водой с добавлением спиртового уксуса (на 1 литр воды - 3-4 ложки уксуса).
Уксус виноградный (4% уксусной кислоты)
Виноградный уксус широко используется ведущими поварами не только Словении, но и всего мира. В Словении его традиционно используют при приготовлении различных овощных и сезонных салатов (2-3 ст. ложки на салатницу), т.к. он придает неповторимый и изысканный вкус блюду. Также виноградный уксус прекрасно сочетается с различными рыбными салатами и блюдами из морских продуктов. При приготовлении шашлыков из различных сортов мяса, но особенно из свинины, виноградный уксус просто незаменим.
Уксусная кислота применяется также для производства лекарственных средств.
Таблетки Аспирина (ЭС) содержат активный ингредиент ацетилсалициловую кислоту, которая представляет собой уксусный эфир салициловой кислоты.
Ацетилсалициловая кислота производится путём нагревания салициловой кислоты с безводной уксусной кислотой в присутствии небольшого количества серной кислоты (в качестве катализатора).
При нагревании с гидроксидом натрия (NaOH) в водном растворе ацетилсалициловая кислота гидролизуется до салицилата натрия и ацетата натрия. При закислении среды салициловая кислота выпадает в осадок и может быть идентифицирована по температуре плавления (156-1600С). Другим методом идентификации салициловой кислоты, образующейся при гидролизе, является окрашивание её раствора в тёмно-фиолетовый цвет при добавлении хлорида железа (FeCl3). Уксусная кислота, присутствующая в фильтрате, превращается при нагревании с этанолом и серной кислотой в этоксиэтанол, который можно легко распознать по его характерному запаху. Кроме того, ацетилсалициловая кислота может быть идентифицирована при помощи различных хроматографических методов.
Ацетилсалициловая кислота кристаллизуется с образованием бесцветных моноклинных многогранников или игл, немного кислых на вкус. Они стабильны в сухом воздухе, однако во влажной среде постепенно гидролизуются до салициловой кислоты и уксусной кислоты (Leeson и Mattocks, 1958; Stempel, 1961). Чистое вещество представляет собой белый кристаллический порошок, почти не обладающий запахом. Запах уксусной кислоты свидетельствует о том, что вещество начало гидролизоваться. Ацетилсалициловая кислота подвергается эстерификации под действием щелочных гидроксидов, щелочных бикарбонатов, а также в кипящей воде.
Ацетилсалициловая кислота оказывает противовоспалительное, жаропонижающее, а также болеутоляющее действие, и ее широко применяют при лихорадочных состояниях, головной боли, невралгиях и др. и в качестве противоревматического средства.
Уксусная кислота используется в и химической промышленности (производство ацетилцеллюлозы, из которой получают ацетатное волокно, органическое стекло, киноплёнку; для синтеза красителей, медикаментов и сложных эфиров), в производстве негорючих пленок, парфюмерных продуктов, растворителей, при синтезе красителей, лекарственных веществ, например, аспирина . Соли уксусной кислоты используют для борьбы с вредителями растений.
Заключение
В данной работе были рассмотрены вопросы открытия уксусной кислоты, ее основные свойства, получение и применение.
Итак, уксусная кислота (CH3COOH), бесцветная горючая жидкость с резким запахом, хорошо растворимая в воде. Имеет характерный кислый вкус, проводит электрический ток. Применение уксусной кислоты в промышленности весьма велико.
У ксусная кислота, производимая в России, находится на уровне лучших мировых стандартов, пользуется высоким спросом на мировом рынке и экспортируется во многие страны мира.
Производство уксусной кислоты имеет ряд своих специфических требований, поэтому необходимы специалисты, имеющие широкий опыт не только в области автоматизации производства и управления процессами, но и четко понимающие специальные требования этой отрасли промышленности.
Список использованной литературы
1. Артеменко, Александр Иванович. Справочное руководство по химии/ А.И. Артеменко, И.В. Тикунова, В.А. Малеванный. - 2-е изд., перераб. и доп. - М.: Высшая школа, 2002. - 367 с
2. Ахметов, Наиль Сибгатович. Общая и неорганическая химия: Учебник для студ. хим.-технол. спец. вузов/Ахметов Н.С.-4-е изд./ испр.- М. : Высшая школа, 2002.-743 с.
3. Березин, Борис Дмитриевич. Курс современной органической химии: Учеб. пособие для студ. вузов, обуч. по хим.-технол. спец./ Березин Б.Д., Березин Д.Б.-М.:Высшая школа,2001.-768 с.
4. И. Г. Болесов, Г. С. Зайцева. Карбоновые кислоты и их производные (синтез, реакционная способность, применение в органическом синтезе). Методические материалы по общему курсу органической химии. Выпуск 5. Москва 1997 г.
5. Зоммер К. Аккумулятор знаний по химии. Пер. с нем., 2-е изд. – М.: Мир, 1985. – 294 с.
6. Караханов Э.А. Синтез-газ как альтернатива нефти. I. Процесс Фишера-Тропша и оксо-синтез // Соросовский Образовательный Журнал. 1997. № 3. С. 69-74.
Еще из раздела Химия:
- Контрольная работа: Хімічні методи виробництва водню і азотоводневої суміші
- Реферат: Ректификационная установка непрерывного действия для разделения 4,1 т/ч бинарной смеси ацетон - этанол
Курсовой проект по ОХТ
«Промышленный способ получения уксусной кислоты»
Введение
Уксусная (этановая) кислота - это органическое вещество с молекулярной формулой CH3COOH (сокращенно - AcOH). Является предельной слабой одноосновной кислотой. Соли уксусной кислоты и ее сложные эфиры называются ацетатами .
Уксус (раствор уксусной кислоты) известен еще с давних времен в качестве продукта брожения. В древности (ок. III в. до н.э.) уксус применялся для получения свинцовых белил. В настоящее время у уксусной кислоты есть три основных применения: во-первых, в роли растворителя для некоторых органических синтезов, во-вторых, как слабо кислый реагент (для гашения образующихся основных продуктов и др.), и, наконец, в-третьих, для производства важных производных, таких как хлорангидрид или ангидрид уксусной кислоты , а так же её амид и прочее. Хлорангидрид и ангидрид уксусной кислоты являются важными ацилирующими агентами, часто применяющимися в органическом синтезе.
Растворы уксусной кислоты, применяющиеся в пищевой промышленности (а также в бытовой кулинарии и засолке) имеют названия уксус (3-15%) и уксусная эссенция (70-80%). Абсолютная уксусная кислота (ок. 99,8%) называется ледяной , т.к. при замерзании она образует массу, напоминающую лёд.
Объёмы производства уксусной кислоты составляют примерно 5 млн. т./год, причем около 50% производится по методу Кольбе (см. ниже) .
. Физико-химические свойства
При н.у. уксусная кислота представляет собой бесцветную жидкость с крайне резким запахом. Далее в таблице сведены основные физические константы уксусной кислоты.
Mr, г/мольp, г/см3Tплав., оСТкип., оСКрит. точкаСмол., Дж/моль*КДНо, кДж/мольрКаn60,051,049216,75118,1321,6 оС 5,79 МПа123,4-4874,761,372
Уксусная кислота амбидентна в отношении растворителей, т.к. имеет в своем составе полярную группу (-COOH) и неполярную (-CH3). Таким образом, она прекрасно растворима в воде и в некоторых органических растворителях. Также она образует двойные и тройные азеотропы типа «уксусная кислота-вода-органический растворитель».
Уксусная кислота является слабой органической кислотой. Она способна реагировать с активными металлами с выделением водорода:
Превращаться в производные кислот под действием соответствующих реагентов (важные реакции в орг. синтезе):
а) в галогенангидриды
б) в сложные эфиры
в) в амиды
Восстанавливаться в этиловый спирт:
А также вступать в реакции замещения по метильной группе, из которых наиболее важной является реакция Геля-Фольгарда-Зелинского, использующаяся для получения важной аминокислоты - глицина:
Причем с каждым последующим замещением, за счет индуктивного эффекта галогена, увеличивается сила кислоты. Так, например, трифторуксусная кислота по своей силе близка к минеральным кислотам .
. Способы получения
Наиболее выгодный и очевидный химический способ получения уксусной кислоты заключается в окислении соответствующего альдегида (ацетальдегида или же этаналя ), который, в свою очередь, получается одним из двух способов: гидратацией ацетилена в присутствии солей ртути (II) (реакция Чугаева), или окислением (дегидрированием) этилового спирта над раскалённой медью:
Ацетальдегид сам по себе легко окисляется кислородом воздуха и медленно превращается в уксусную кислоту.
Первый способ получения этаналя по реакции Чугаева не выгоден по многим причинам, среди которых работа с взрывоопасным ацетиленом, загрязнение продукта ядовитыми солями ртути, большие объемы реакторов и проч. Наиболее распространен второй способ получения из этилового спирта (который производится в огромных количествах и сравнительно дешев).
Полученный ацетальдегид окисляется кислородом в присутствии катализатора - солей марганца (II). Именно этот метод и будет рассматриваться в дальнейшем.
Более современным является метод каталитического карбонилирования метанола (метод Кольбе) по реакции:
Этот метод позволяет достигать выходов порядка 99% по метанолу и 90% по СО. Он заключается в барботаже монооксида углерода при температуре 180°С и давлениях 200-700 атм через смесь реагентов. Катализаторами являются иодиды кобальта или родия, а так же, реже, соединения иридия. На данный момент по этому методу получают около 50% всей уксусной кислоты, производимой в мире.
Существуют так же и биохимические методы (т.е. посредством брожения сахаров), однако, они редко применяются, в основном из-за их малой производительности и сложности разделения полученной смеси продуктов.
. Обоснование выбора технологического процесса методом окисления этаналя
Данный метод обладает рядом положительных качеств, таких как:
)Дешёвые исходные реагенты
)Высокая производительность
)Относительно невысокие энергетические затраты (50-60 оС)
)Высокие выходы по исходным реагентам
)Высокая степень превращения и селективность процесса
)Относительно простое разделение смеси
Реакция проводится в колонне барботажного типа. Повышенная температура необходима для предотвращения побочной реакции образования перекисей (из-за которых может образовываться взрывоопасная смесь). Верхний предел температуры определяется летучестью ацетальдегида. Уксусная кислота является не только продуктом реакции, но и растворителем, что значительно упрощает процесс.
Основные технологические показатели процесса сведены в таблицу ниже:
. Технологическая схема процесса
Ниже представлена упрощенная технологическая схема получения уксусной кислоты окислением ацетальдегида. Обозначения, приведенные на схеме, сведены в таблицы.
Исходная смесь (I) поступает в теплообменник (1), где подогревается до температуры реакции (50-80 оС). Обогрев производится греющим паром (IX), который затем в виде конденсата (X) отводится из межтрубного пространства. Подача альдегида производится центробежными насосами (5) и регулируется вентилями.
Нагретый альдегид поступает в барботажную колонну (2), снабженную змеевиковыми холодильниками (реакция - экзотермическая). В колонну продувается технический кислород (II), начинается окисление альдегида.
Полученные продукты в виде паро-жидкостной смеси выводятся через верх колонны и поступают в распределитель (4), после чего, часть реакционной массы поступает в первую ректификационную колонну (3), предназначенную для очистки от легколетучих примесей (выхлопные газы - VII). Далее, остаток реакционной массы (IV) поступает во вторую колонну, где полученная уксусная кислота (V) отводится к потребителю или на склад. Кубовый остаток (VI), содержащий этилидендиацетат также удаляется из колонны. Непрореагировавший ацетальдегид (VIII) возвращается в барботажную колонну, тем самым уменьшая количество изначально необходимого альдегида, для обеспечения заданной производительности (повышается конверсия сырья). .
Таблицы основных потоков и обозначений:
Расчётная часть
. Составление материального баланса
Составление материального баланса является одним из главных пунктов расчета технологических процессов. Его суть заключается в законе сохранения массы (Приход-Уход=0). Благодаря составлению уравнений мат. баланса можно оперировать различными показателями процесса (концентрациями, массовыми потоками и т.д.) для оптимизации процесса.
Начать составлять баланс следует с упрощенной схемы в виде блоков. Каждый из блоков будет включать в себя основную функцию - смешение, окисление или распределение. Для данного процесса блок-схема будет выглядеть следующим образом (состав потоков указан выше в таблице):
Таким образом, видно, что технологическая схема разбивается на четыре основных блока:
1)Блок смешения.
)Блок окисления (непосредственно сама барботажная колонна).
)Блок разделения (первая ректификационная колонна, из которой отводятся легколетучие вещества, выхлопные газы).
)Блок разделения и возвращения непрореагировавшего сырья в первый блок.
Во втором блоке происходит перераспределение масс за счет химических превращений по основной реакции:
СН3СНО + 0,5О2 = СН3СООН
И по двум побочным реакциям образования метилацетата и этилидендиацетата соответственно:
СН3СНО + 1,5О2 = СН3СООСН3 + СО2 + Н2О
СН3СНО + О2 = СН3СН(ООССН3)2 + Н2О
Исходя из заданной производительности по продукту и селективности и степени превращения по ацетальдегиду можно рассчитать необходимое количество этаналя по базисному уравнению:
где N - количество молей исходного ацетальдегида, необходимое для поступления в первый реактор; M - молярная масса продукта (уксусной кислоты); а и с - стехиометрические коэффициенты реагента и продукта,
Следовательно, в блок 1 должно поступать 31,6265 кмоль ацетальдегида. Следует учесть, что ацетальдегид поступает как чистый (исходный), так и обратный (после четвёртого блока) по рециркуляции. Массовый расход составляет:
Рассчитаем также количества образующихся побочных продуктов:
а) метилацетата:
б) этилидендиацетата:
Где 0,5 и 0,33 переводные коэффициенты (с учетом стехиометрии реакции). Рассчитаем количество кислорода, необходимое для реакции (с учетом его конверсии, т.е. не полного превращения):
Технический кислород содержит небольшое количество азота (2,5%), которое следует учитывать:
Непрореагировавший альдегид:
Количество образующегося углекислого газа:
Вода, образовавшаяся по реакциям :
Следует учитывать, что вода так же поступает с исходным сырьем.
Альдегид (в атмосферу):
Альдегид (в 4-ый блок):
Так как весь альдегид, переходящий в блок 4, затем поступает обратно в блок 1, то теперь можно рассчитать количество свежего альдегида, поступающего в 1-ый блок на смешение:
А так же количества примесей (уксусной кислоты и воды) в свежем альдегиде:
Общее количество воды (по реакции и с свежим альдегидом) составляет:
Уксусная кислота образуется в результате реакции и при поступлении с свежим альдегидом:
Часть воды удаляется вместе с уксусной кислотой (0,2% по массе):
Баланс по воде составляется следующим образом: образованная по реакции + с свежим альдегидом - с кислотой - в атмосферу = 0. Тогда:
Все расчетные значения для удобства сводятся в таблицу потоков и таблицу материального баланса.
*Примечание №1: метилацетат имеет температуру кипения 57 оС и является легколетучим веществом, поэтому он удаляется с выхлопными газами т.е. в третьем блоке (первой ректификационной колонне).
*Примечание №2: следует также учитывать, что в колонне находится постоянное количество уксусной кислоты (в качестве растворителя), и рециркулирующий ацетальдегид.
Заключение
кислота альдегид этаналь
В заключение следует отметить, что данный метод является практически основным в получении уксусной кислоты. В последнее время он все чаще замещается методом Кольбе (карбоксилированием метилового спирта), который даёт более высокие выходы по исходным реагентам.
Данный метод обладает и недостатками, такими как, например, выброс в атмосферу непрореагировавшего ацетальдегида и метилацетата, применение повышенного давления, образование побочных продуктов и пр.
Тем не менее, около 50% всей уксусной кислоты, производимой в мире, получают именно таким способом, используя в качестве катализатора ацетаты марганца (II). В целом, подобный метод является одним из наиболее удобных и выгодных для технологии.
Уксусная кислота является одним из наиболее ходовых и используемых продуктов сырья, а так же крайне востребована в пищевой и химической промышленности.
Список использованной литературы
1) «Экологический фактор или окружающая среда как стимул эволюции промышленной химии». Роджер А. Шелдон
) «Органическая химия». Моррисон Р., Бойд Р., 1974 г.
) «Механизмы реакций в органической химии». Сайкс П., 1991 г.
) «Сборник заданий и методических указаний по расчету материального баланса химико-технологических производств». МИТХТ, 2008 г.
Дополнительная литература:
5) «Общий курс процессов и аппаратов химической технологии». Айнштейн В.Г., Захаров М.К., 1999 г.
) «Краткий справочник физико-химических величин». Равдель А.А., 1999 г.
) «Схемы химико-технологических процессов». Носов Г.А., Вышнепольский В.И., Лапшенков Г.И., 2011 г.
Длина и расстояние Масса Меры объема сыпучих продуктов и продуктов питания Площадь Объем и единицы измерения в кулинарных рецептах Температура Давление, механическое напряжение, модуль Юнга Энергия и работа Мощность Сила Время Линейная скорость Плоский угол Тепловая эффективность и топливная экономичность Числа Единицы измерения количества информации Курсы валют Размеры женской одежды и обуви Размеры мужской одежды и обуви Угловая скорость и частота вращения Ускорение Угловое ускорение Плотность Удельный объем Момент инерции Момент силы Вращающий момент Удельная теплота сгорания (по массе) Плотность энергии и удельная теплота сгорания топлива (по объему) Разность температур Коэффициент теплового расширения Термическое сопротивление Удельная теплопроводность Удельная теплоёмкость Энергетическая экспозиция, мощность теплового излучения Плотность теплового потока Коэффициент теплоотдачи Объёмный расход Массовый расход Молярный расход Плотность потока массы Молярная концентрация Массовая концентрация в растворе Динамическая (абсолютная) вязкость Кинематическая вязкость Поверхностное натяжение Паропроницаемость Паропроницаемость, скорость переноса пара Уровень звука Чувствительность микрофонов Уровень звукового давления (SPL) Яркость Сила света Освещённость Разрешение в компьютерной графике Частота и длина волны Оптическая сила в диоптриях и фокусное расстояние Оптическая сила в диоптриях и увеличение линзы (×) Электрический заряд Линейная плотность заряда Поверхностная плотность заряда Объемная плотность заряда Электрический ток Линейная плотность тока Поверхностная плотность тока Напряжённость электрического поля Электростатический потенциал и напряжение Электрическое сопротивление Удельное электрическое сопротивление Электрическая проводимость Удельная электрическая проводимость Электрическая емкость Индуктивность Американский калибр проводов Уровни в dBm (дБм или дБмВт), dBV (дБВ), ваттах и др. единицах Магнитодвижущая сила Напряженность магнитного поля Магнитный поток Магнитная индукция Мощность поглощенной дозы ионизирующего излучения Радиоактивность. Радиоактивный распад Радиация. Экспозиционная доза Радиация. Поглощённая доза Десятичные приставки Передача данных Типографика и обработка изображений Единицы измерения объема лесоматериалов Вычисление молярной массы Периодическая система химических элементов Д. И. Менделеева
Химическая формула
Молярная масса CH 3 COOH, уксусная кислота 60.05196 г/моль
12,0107+1,00794·3+12,0107+15,9994+15,9994+1,00794
Массовые доли элементов в соединении
Использование калькулятора молярной массы
- Химические формулы нужно вводить с учетом регистра
- Индексы вводятся как обычные числа
- Точка на средней линии (знак умножения), применяемая, например, в формулах кристаллогидратов, заменяется обычной точкой.
- Пример: вместо CuSO₄·5H₂O в конвертере для удобства ввода используется написание CuSO4.5H2O .
Калькулятор молярной массы
Моль
Все вещества состоят из атомов и молекул. В химии важно точно измерять массу веществ, вступающих в реакцию и получающихся в результате нее. По определению моль - это количество вещества, которое содержит столько же структурных элементов (атомов, молекул, ионов, электронов и других частиц или их групп), сколько содержится атомов в 12 граммах изотопа углерода с относительной атомной массой 12. Это число называется постоянной или числом Авогадро и равно 6,02214129(27)×10²³ моль⁻¹.
Число Авогадро N A = 6.02214129(27)×10²³ моль⁻¹
Другими словами моль - это количество вещества, равное по массе сумме атомных масс атомов и молекул вещества, умноженное на число Авогадро. Единица количества вещества моль является одной из семи основных единиц системы СИ и обозначается моль. Поскольку название единицы и ее условное обозначение совпадают, следует отметить, что условное обозначение не склоняется, в отличие от названия единицы, которую можно склонять по обычным правилам русского языка. По определению один моль чистого углерода-12 равен точно 12 г.
Молярная масса
Молярная масса - физическое свойство вещества, определяемое как отношение массы этого вещества к количеству вещества в молях. Говоря иначе, это масса одного моля вещества. В системе СИ единицей молярной массы является килограмм/моль (кг/моль). Однако химики привыкли пользоваться более удобной единицей г/моль.
молярная масса = г/моль

Молярная масса элементов и соединений
Соединения - вещества, состоящие из различных атомов, которые химически связаны друг с другом. Например, приведенные ниже вещества, которые можно найти на кухне у любой хозяйки, являются химическими соединениями:
- соль (хлорид натрия) NaCl
- сахар (сахароза) C₁₂H₂₂O₁₁
- уксус (раствор уксусной кислоты) CH₃COOH
Молярная масса химических элементов в граммах на моль численно совпадает с массой атомов элемента, выраженных в атомных единицах массы (или дальтонах). Молярная масса соединений равна сумме молярных масс элементов, из которых состоит соединение, с учетом количества атомов в соединении. Например, молярная масса воды (H₂O) приблизительно равна 2 × 2 + 16 = 18 г/моль.
Молекулярная масса

Молекулярная масса (старое название - молекулярный вес) - это масса молекулы, рассчитанная как сумма масс каждого атома, входящего в состав молекулы, умноженных на количество атомов в этой молекуле. Молекулярная масса представляет собой безразмерную физическую величину, численно равную молярной массе. То есть, молекулярная масса отличается от молярной массы размерностью. Несмотря на то, что молекулярная масса является безразмерной величиной, она все же имеет величину, называемую атомной единицей массы (а.е.м.) или дальтоном (Да), и приблизительно равную массе одного протона или нейтрона. Атомная единица массы также численно равна 1 г/моль.
Похожие статьи
-
Английский - часы, время
Всем кто интересуется изучением английского языка, приходилось сталкиваться со странными обозначениями p. m. и a. m , и вообще, везде, где упоминается о времени, почему-то используется всего 12 часовой формат . Наверное, для нас живущих...
-
"Алхимия на бумаге": рецепты
Doodle Alchemy или Алхимия на бумаге на Андроид — интересная головоломка с красивой графикой и эффектами. Узнайте как играть в эту удивительную игру, а также найдите комбинации элементов для прохождения игры Алхимия на бумаге. Игра...
-
Не запускается Batman: Arkham City (Batman: Аркхем Сити)?
Если вы столкнулись с тем, что Batman: Arkham City тормозит, вылетает, Batman: Arkham City не запускается, Batman: Arkham City не устанавливается, в Batman: Arkham City не работает управление, нет звука, выскакивают ошибки, в Batman:...
-
Как отучить от игровых автоматов человека Как отучить играть в азартные игры
Вместе с психотерапевтом московской клиники Rehab Family и специалистом в терапии игромании Романом Герасимовым «Рейтинг Букмекеров» проследил путь игромана в ставках на спорт – от формирования зависимости до обращения к врачу,...
-
Ребусы Занимательные ребусы головоломки загадки
Игра "Загадки Ребусы Шарады": ответ к разделу "ЗАГАДКИ" Уровень 1 и 2 ● Не мышь, не птица - в лесу резвится, на деревьях живёт и орешки грызёт. ● Три глаза - три приказа, красный - самый опасный. Уровень 3 и 4 ● Две антенны на...
-
Сроки поступления средств на ЯД
СКОЛЬКО ИДУТ ДЕНЬГИ НА СЧЕТ КАРТЫ СБЕРБАНКА Важные параметры платежных операций – сроки и тарифы зачисления денежных средств. Эти критерии прежде всего зависят от выбранного способа перевода. Какие условия перечисления денег между счетам
