ძმარმჟავას წყალი. ძმარმჟავას გამოყენება
სახელი:
ძმარმჟავა(ეთანოინის მჟავა) არის ალიფატური სერიის მონობაზური კარბოქსილის მჟავა.
ქიმიური ფორმულა:
გახსნის ისტორია:
ძმარმჟავა ცნობილია უძველესი დროიდან, რადგან წარმოიქმნება ღვინოების დამჟავებისას (ღვინის ძმარი).
მაგრამ მეცნიერები ძმარმჟავას სტრუქტურით და მისი წარმოშობის მიზეზით დაინტერესდნენ მხოლოდ დიუმას ცერის წესის სენსაციური გამოქვეყნების შემდეგ ორგანულ ნაერთებში წყალბადის ქლორით ჩანაცვლების შესახებ. მანამდე ქიმიაში დომინირებდა იენს იაკობ ბერცელიუსის მიერ წამოყენებული თეორია. მან ელემენტები დაყო ელექტროდადებითად და ელექტროუარყოფითად და მთლიანად უარყო წყალბადის და ქლორის ჩანაცვლება, შესაბამისად, შეუცვლელად. ქიმიური სტრუქტურანივთიერებები.
თავის 1839 წლის ნაშრომში დიუმამ წარუდგინა მოხსენება შვედეთის აკადემიას, რომელშიც მან აკურთხა ორგანული ნივთიერებების და განსაკუთრებით ძმარმჟავას ფორმულირების წესის საწყისი პრინციპები: „არაორგანულ ქიმიაში ჩვენ ვხელმძღვანელობთ იზომორფიზმით, თეორია, რომელიც დაფუძნებულია ფაქტებზე, როგორც ცნობილია, რამდენიმე მათგანი ეთანხმება ელექტროქიმიურ თეორიებს. ორგანულ ქიმიაში ჩანაცვლების თეორია ერთსა და იმავე როლს ასრულებს... და შესაძლოა, მომავალი გვიჩვენებს, რომ ორივე შეხედულება უფრო მჭიდრო კავშირშია, რომ ისინი გამომდინარეობენ ერთი და იგივე მიზეზებიდან და შეიძლება განზოგადდეს ერთი და იგივე სახელით.
მას რამდენიმე წელი დასჭირდა ამ დასკვნამდე მისასვლელად. დიუმამ დაიწყო თავისი პირველი ექსპერიმენტები ძმარმჟავას შესწავლით და მისი ქლოროძმარმჟავად გადაქცევით. წყალბადი ამ რეაქციაში მთლიანად ჩანაცვლებულია ქლორით, 1:1 თანაფარდობით და რაც მთავარია, ძირითადი ელემენტების დაკარგვის გარეშე. ქიმიური თვისებებიდა მატერიის ურთიერთობა კლასთან. შემდგომმა ექსპერიმენტებმა წყალბადის იოდითა და ბრომით ჩანაცვლებით საბოლოოდ დაარწმუნა მეცნიერი ამაში.
დასკვნა არაორგანული და ორგანული ნაერთების წარმოქმნას შორის ფუნდამენტური განსხვავების შესახებ რევოლუციური აღმოჩნდა.
ამასთან, ბერცელიუსი, რომელიც იცავს თავის თეორიას, მოჰყავს ოქსილის მჟავის მაგალითი და მიღებული მარილი ქლორიდთან შერწყმისას, რაც ნიშნავს მჟავე თვისებების დაკარგვას. ის ამტკიცებს, როგორც ორგანული, ისე არაორგანული ნაერთების მაგალითის გამოყენებით, რომ მათ ჟანგბადის შემცველ ნაწილს შეუძლია რეაგირება მოახდინოს ფუძეებთან და დაკარგოს ისინი ქლორის შემცველ ნაწილთან კონტაქტის დაკარგვის გარეშე. სწორედ ეს ასპექტია, ქიმიკოსის აზრით, დიუმას მიერ თავის ექსპერიმენტებში დაშვებული მთავარი გამოტოვება, ვინაიდან. მან არც უარყო და არც დაადასტურა ეს ცნობილი ფაქტი.
დიუმას მიერ მიღებული შედეგების როგორმე ახსნის მიზნით, ბერცელიუსი აყენებს ვარაუდს: „დიუმას ქლოროძმარმჟავა,
აშკარად მიეკუთვნება ნაერთების ამ კლასს; მასში ნახშირბადის რადიკალი არის დაკავშირებული
ჟანგბადიც და ქლორიც. შესაბამისად, ეს შეიძლება იყოს ოქსილის მჟავა
რომელშიც ჟანგბადის ნახევარი ჩანაცვლებულია ქლორით, ანუ 1 ატომის ნაერთით
ოქსილის მჟავას (მოლეკულები) ნახშირბადის სესქიქლორიდის 1 ატომით (მოლეკულა)
C2Cl6. პირველი ვარაუდი არ შეიძლება იქნას მიღებული, რადგან ის აღიარებს
ქლორის 11/2, ჟანგბადის ატომების ჩანაცვლების შესაძლებლობა (ბერზელიუსის მიხედვით, ოქსიალი
მჟავა იყო C2O3.). სამაგიეროდ, დიუმა მთლიანად ეკიდება მესამე იდეას
შეუთავსებელია ზემოთ ჩამოთვლილ ორთან, რომლის მიხედვითაც ქლორი არ ცვლის ჟანგბადს, მაგრამ
ელექტროდადებითი წყალბადი, რომელიც ქმნის ნახშირწყალბადს C4Cl6, რომელსაც აქვს იგივე
რთული რადიკალის თვისებები, როგორიცაა C4H6 ან აცეტილი, და სავარაუდოდ შეუძლია 3
ჟანგბადის ატომები მისცეს მჟავას იდენტური თვისებებით U., მაგრამ, როგორც ხედავთ
შედარებიდან (მათი ფიზიკური თვისებების), მისგან სრულიად განსხვავებული"
მაგრამ დიუმას მიერ დარგულმა თესლებმა ყლორტები მისცეს. ახლა ბევრმა მეცნიერმა ზურგი აქცია ბერცელიუსის თეორიას და განაგრძო ინოვაციები. ასე რომ, ჩარლზ ფრედერიკ ჟერარდმა პირველად, რადიკალების თეორიის საწინააღმდეგოდ (რომლის შემქმნელი და მიმდევარი იყო ბერცელიუსი), დაადგინა, რომ რადიკალები დამოუკიდებლად არ არსებობენ, არამედ არიან ატომური ჯგუფები - „ნარჩენები“, რომელთა კომბინაცია ქმნის მოლეკულას. . 1851 წელს თავის ნარკვევში "მჟავების საფუძვლების შესახებ" მან შეიმუშავა ტიპების თეორია, რომლის მიხედვითაც ყველა ქიმიური ნაერთი შეიძლება დაიყოს ოთხი ტიპის წარმოებულებად - წყალბადი, წყალბადის ქლორიდი, წყალი და ამიაკი. კერძოდ, გაჩნდა აზრი ტრიქლოროძმარმჟავას და ძმარმჟავას კონსტიტუციის მსგავსებაზე. თავის დასაცავად ბერცელიუსი პასუხობს: „ჟერარდმა გამოთქვა ახალი შეხედულება ალკოჰოლის, ეთერისა და მათი შემადგენლობის შესახებ.
წარმოებულები; ეს არის შემდეგი: ცნობილია ქრომის, ჟანგბადის და ქლორის ნაერთი
ფორმულა \u003d CrO2Cl2, ქლორი ცვლის მასში ჟანგბადის ატომს (იგულისხმება
ბერზელიუსის 1 ჟანგბადის ატომი ქრომის ანჰიდრიდი - CrO3). U. მჟავა C4H6 + 3O
შეიცავს ოქსილის მჟავას 2 ატომს (მოლეკულას), რომელთაგან მთელი
ჟანგბადი ჩანაცვლებულია წყალბადით = C2O3+C2H6. მაგრამ რიცხვების ასეთი თამაში არ ფლობდა თეორიის ავტორიტეტს და ერთი წლის შემდეგ დიუმამ გამანადგურებელი დარტყმა მიაყენა, შეიმუშავა ტიპების თეორია, გამოიკვლია ტრიქლოროძმარმჟავას და ძმარმჟავას მსგავსი თვისებები დაშლის რეაქციაში, გავლენის ქვეშ. ტუტეები.
თავის მხრივ, ლიბიგი და გრეჰემი საჯაროდ საუბრობდნენ ამის სასარგებლოდ
ჩანაცვლების თეორიის საფუძველზე მიღწეული უფრო დიდი სიმარტივე განხილვისას
მიღებული ჩვეულებრივი ეთერის ქლორის წარმოებულები და ფორმული და U. მჟავა ეთერები
მალაგუტი.
ბერცელიუსი, დაემორჩილა ახალი ფაქტების ზეწოლას, მე-5 გამოცემაში. მისი
"Lehrbuch der Chemie" (წინასიტყვა აღინიშნა 1842 წლის ნოემბერი), 709 გვერდზე,
დაივიწყა ჟერარდის მკვეთრი მიმოხილვა, მან შეძლო შემდეგი დაწერა: „თუ ჩვენ
გავიხსენოთ ქლორის ზემოქმედებით U. მჟავის ტრანსფორმაცია (ტექსტში დაშლა).
ქლოროოქსალიუმის მჟავა (ქლოროქსალსაურე - ქლოროქსალზაურე - ბერცელიუსი უწოდებს
ტრიქლოროძმარმჟავა. , შემდეგ გამოჩნდება
შესაძლებელია U. მჟავის შემადგენლობის სხვა ხედვა, კერძოდ, ის შეიძლება იყოს კომბინირებული ოქსილის მჟავა, რომელშიც კომბინირებული ჯგუფი (Paarling) არის C2H6, ისევე როგორც ქლოროოქსალიუმის მჟავაში კომბინირებული ჯგუფი არის C2Cl6, შემდეგ კი ქლორის მოქმედება U. მჟავა შედგებოდა მხოლოდ C2H6-ის C2Cl6-ად გადაქცევაში. ნათელია, რომ შეუძლებელია გადაწყვიტოს, არის თუ არა ასეთი წარმოდგენა უფრო სწორი ..., თუმცა, სასარგებლოა ყურადღების მიქცევა ამის შესაძლებლობაზე.
მაგრამ ტიპების თეორიის მომხრეთა პოლკში ყველაფერი ჩამოვიდა. კოლბის მუშაობის ამოსავალი წერტილი იყო კრისტალური ნივთიერების, CCl4SO2 შემადგენლობის შესწავლა, რომელიც ადრე მიიღეს ბერცელიუსმა და მარსმა CS2-ზე aqua regia-ს მოქმედებით და წარმოიქმნა კოლბის მიერ CS2-ზე სველი ქლორის მოქმედებით. გარდაქმნების მახლობლად, კოლბემ აჩვენა, რომ ეს
სხეული წარმოადგენს, თანამედროვე თვალსაზრისით, ქლორის ანჰიდრიდს
ტრიქლორმეთილსულფონის მჟავა, CCl4SO2 \u003d CCl3.SO2Cl, რომელსაც ტუტეების გავლენის ქვეშ შეუძლია მიიღოს შესაბამისი მჟავის მარილები - CCl3.SO2 (OH), რომელიც თუთიის გავლენით პირველ რიგში ცვლის Cl ატომს წყალბადით, წარმოქმნის. მჟავა CHCl2.SO2 (OH) ბერზელიუსის ჰიდრატირებული წყალი, როგორც ყოველთვის, მიუღებელია
მხედველობაში.), შემდეგ კი სხვა, რომელიც წარმოქმნის მჟავას CH2Cl.SO2 (OH) [კოლბის მიხედვით -
Chlorelaylunterschwefelsaure], და ბოლოს, როდესაც აღდგება დენით ან კალიუმით
ამალგამი (რეაქცია ცოტა ხნის წინ გამოიყენა მელსანსმა
ტრიქლოროძმარმჟავას რედუქცია ძმარმჟავამდე.) ცვლის წყალბადით და სამივე
Cl ატომი, რომელიც ქმნის მეთილსულფონის მჟავას. CH3.SO2(OH) [კოლბეს მიხედვით -
Methylunterschwefelsaure].
ამ ნაერთების ანალოგია ქლოროძმარმჟავებთან
უნებურად მოჰკრა თვალი; მართლაც, მაშინდელი ფორმულებით, ორი
პარალელური სერიები, როგორც ჩანს შემდეგი ცხრილიდან: H2O+C2Cl6.S2O5
H2O+C2Cl6.C2O3 H2O+C2H2Cl4.S2O5 H2O+C2H2Cl4.C2O3 H2O+C2H4Cl2.S2O5
H2O+C2H4Cl2.C2O3 H2O+C2H6.S2O5 H2O+C2H6.C2O3 ამას არ გაურბოდა კოლბე,
ვინც აღნიშნავს (I. გვ. გვ. 181): „ზემოთ აღწერილ კომბინირებულ გოგირდმჟავებს
მჟავები და უშუალოდ ქლოროკარბონის გოგირდმჟავაში (ზემოთ -
H2O + C2Cl6.S2O5) უერთდება ქლოროოქსალის მჟავას, რომელიც ასევე ცნობილია როგორც
ქლოროძმარმჟავა. თხევადი ქლოროკარბონი - CCl (Cl=71, C=12; ახლა ვწერთ
C2Cl4 არის ქლოროეთილენი.), ცნობილია, რომ გარდაიქმნება შუქზე გავლენის ქვეშ
ქლორი - ჰექსაქლოროეთანი და შეიძლება მოსალოდნელი იყოს, რომ თუ იგი ერთდროულად დაექვემდებარა წყლის მოქმედებას, მაშინ ის, როგორც ბისმუტის ქლორიდი, ქლორის ანტიმონი და ა.შ., წარმოქმნის დროს, ჩაანაცვლებს ქლორს ჟანგბადით. გამოცდილებამ დაადასტურა ვარაუდი.„შუქის მოქმედებით და
ქლორი C2Cl4-ზე, რომელიც წყლის ქვეშ იყო, კოლბემ მიიღო ჰექსაქლოროეთანთან ერთად
და ტრიქლოროძმარმჟავას და გამოხატა ტრანსფორმაცია შემდეგნაირად: (ვინაიდან C2Cl4
შეიძლება მიღებულ იქნას CCl4-დან გახურებულ) მილში გავლის გზით და CCl4
წარმოიქმნება CS2-ზე Cl2-ის გახურებისას მოქმედებით, მაშინ იყო კოლბის რეაქცია
U. მჟავის პირველი სინთეზი ელემენტებიდან.) „წარმოიქმნება თუ არა ერთდროულად
და თავისუფალი ოქსილის მჟავა, ძნელია გადაწყვიტოს, რადგან სინათლის ქლორის დაუყოვნებლივ
იჟანგება მას U. მჟავად "...
ბერცელიუსის შეხედულება ქლოროძმარმჟავაზე
„გასაკვირველია (auf eine tiberraschende Weise) დადასტურებულია
კომბინირებული გოგირდმჟავების თვისებების არსებობა და პარალელურობა და, როგორც ი
ჩანს (ამბობს Kolbe I. გვ. გვ. 186), სცილდება ჰიპოთეზების სფეროს და
იძენს ალბათობის მაღალ ხარისხს.
მისი შორსმჭვრეტელობა ბუნების შემდგომი აღმოჩენების შესახებ ორგანული მჟავებიდასტურდება სტატიით, რომელშიც ექსპერიმენტებზე დაყრდნობით წერს: „არა
დაუჯერებელია, რომ მომავალში იძულებული ვიქნებით მივიღოთ კომბინირებული მჟავები
იმ ორგანული მჟავების მნიშვნელოვანი რაოდენობა, რომელშიც ამჟამად, იმის გამო
ჩვენი ინფორმაციის შეზღუდვები - ჩვენ ვიღებთ ჰიპოთეტურ რადიკალებს ... ".
მისთვის დამახასიათებელია რადიკალების თეორიაც, რაც ადასტურებს უკვე ითქვა, ასევე დასძენს: „რაც შეეხება ამ შერეულ მჟავებში ჩანაცვლების ფენომენებს, ისინი იღებენ მარტივ ახსნას იმ ვითარებაში, რომ სხვადასხვა, ალბათ იზომორფულ ნაერთებს შეუძლიათ შეცვალონ. ერთმანეთის როლში შემაერთებელი ჯგუფები მნიშვნელოვნად არ ცვლის მათთან ერთად სხეულის მჟავე თვისებებს!
ამ მოსაზრების შემდგომ ექსპერიმენტულ დადასტურებას ვპოულობთ ფრანკლენდისა და კოლბის სტატიაში: „იმ აზრზე დაყრდნობით, რომ სერიის ყველა მჟავა
(CH2)2nO4, აგებული მეთილის ოქსილის მჟავის მსგავსად (ახლა ვწერთ CnH2nO2 და
ჩვენ ვუწოდებთ მეთილის ოქსილის მჟავას - ძმარმჟავას. კომბინირებული in
ჭიანჭველა მჟავა, წყალბადი მონაწილეობს რეაქციაში მხოლოდ იმიტომ, რომ აერთიანებს
ციანიდი, ქმნის ჰიდროციანმჟავას: საპირისპირო განათლებაჭიანჭველა მჟავისგან
ტუტეების გავლენის ქვეშ ჰიდროციანური სხვა არაფერია, თუ არა გამეორება
წყალში გახსნილი ციანიდის ცნობილი გარდაქმნა ოქსილის მჟავად და ამიაკად,
ამ ერთადერთი განსხვავებით; რომ წარმოქმნის დროს ოქსილის მჟავა ერწყმის
ჰიდროციანმჟავა."
ის ფაქტი, რომ ბენზოლის ციანიდს (C6H5CN), მაგალითად, ფელინგის მიხედვით, არ აქვს მჟავე თვისებები და არ წარმოქმნის პრუსიულ ლურჯს, კოლბისა და ფანკლენდის აზრით, შეიძლება პარალელურად იყოს ეთილის ქლორიდის უუნარობა აგნო3-თან რეაქციისთვის, და მათი მითითების სისწორე კოლბე და
ფრანკლენდი ამტკიცებს სინთეზით ნიტრილების მეთოდით (მათ მიიღეს ნიტრილები
სერნოვიკური მჟავების დისტილაცია KCN-ით (დუმას და მალაგუტის მეთოდი Leblanc-ით):
R".SO3 (OH) + KCN \u003d R.CN + KHSO4) U., პროპიონური (შესაბამისად, მეტ-აცეტონი,) და
კაპრონის მჟავა.
შემდეგ, მომდევნო წელს, კოლბმა ელექტროლიზა გაუკეთა ტუტეს
მონობაზური გაჯერებული მჟავების მარილები და მისი სქემის მიხედვით დაფიქსირდა ზე
ამავდროულად, ძმარმჟავას ელექტროლიზის დროს წარმოიქმნება ეთანის, ნახშირბადის მჟავა და
წყალბადი:
H2O+C2H6.C2O3=H2+,
ხოლო ვალერინის ელექტროლიზში - ოქტანი, ნახშირმჟავა და წყალბადი: H2O + C8H18.C2O3 \u003d H2 +.
კოლბის ნამუშევრები, ძმარმჟავას სტრუქტურა და ამავდროულად ყველა
სხვა ორგანული მჟავები საბოლოოდ გაირკვა და შემდგომი ქიმიკოსების როლი
შემცირდა მხოლოდ დაყოფამდე - თეორიული მოსაზრებებიდან და ჟერარდის ავტორიტეტიდან გამომდინარე,
კოლბის ფორმულები ნახევრად და მათი თარგმნა სტრუქტურული შეხედულებების ენაზე,
რის გამოც ფორმულა C2H6.C2O4H2 გადაიქცა CH3.CO(OH).
მიღების გზები:
ძმარმჟავას წარმოების ძირითადი ტექნიკური მეთოდია აცეტალდეჰიდის დაჟანგვა ატმოსფერული ჟანგბადით მანგანუმის კატალიზატორების თანდასწრებით.
აცეტალდეჰიდის ძმარმჟავა
ქიმიური თვისებები:
ურთიერთქმედება:
ლითონები
ძმარმჟავა მაგნიუმის აცეტატი
განაცხადი:
ძმარმჟავა ფართოდ გამოიყენება ინდუსტრიაში:
- ხორცისა და თევზის პროდუქტების დაკონსერვება,
- სინთეზური (აცეტატური) ბოჭკოების წარმოება,
- ჰერბიციდების წარმოება,
- არომატული ნივთიერებებისა და გამხსნელების სინთეზი,
- ტყავის, ტექსტილის და სხვა ინდუსტრიებში,
- ფართოდ გამოიყენება ძმარმჟავას მარილები - აცეტატები.
ეჭვგარეშეა, ყველაზე მრავალმხრივი ცნობილი გამხსნელები, რომლებიც დაკავშირებულია ალიფატურ მონობაზურ მჟავებთან, არის კარგად ცნობილი ძმარმჟავა. მას ასევე აქვს სხვა სახელები: ძმრის ესენციაან ეთანოინის მჟავა. ამ ნივთიერების დაბალმა ღირებულებამ და ხელმისაწვდომობამ სხვადასხვა კონცენტრაციებში (3-დან 100%-მდე), მისმა სტაბილურობამ და გაწმენდის სიმარტივემ განაპირობა ის, რომ დღეს ეს არის საუკეთესო და ყველაზე ცნობილი აგენტი, რომელსაც აქვს ნივთიერებების უმეტესობის დაშლის თვისებები. ორგანული წარმოშობა, რომელსაც დიდი მოთხოვნა აქვს ადამიანის საქმიანობის სხვადასხვა სფეროში.
ძმარმჟავა და, შესაბამისად, მისი გამოყენების შესაძლებლობა ცალკეულ ინდუსტრიებში, შეიძლება განსხვავდებოდეს კონცენტრაციით. იგი იყოფა საკვებად, ანუ ძმარი (3-15%) და ტექნიკური - ძმრის ესენცია (70-80%) და ყინული (100%).
როგორც საყოფაცხოვრებო დონეზე, ისე ზოგადად, ქ Კვების ინდუსტრიადიდი მოთხოვნაა დაბალ კონცენტრირებულ ხსნარზე, ძმარმჟავას პროცენტი, რომელშიც დაახლოებით 3-15%-ია. მას აზავებენ მზა კერძებით, გამოიყენება მთელი რიგი პროდუქტების არომატისთვის, შეუცვლელია ხორცისა და თევზის პროდუქტების დასაკონსერვებლად, დამარინადებლად და დამარილებლად და ა.შ.
ტექნიკური ძმარმჟავა 70, ყიდვარომელიც, საკვებისგან განსხვავებით, ვერ მოიძებნება ჩვეულებრივ სასურსათო მაღაზიაში, აქტიურად გამოიყენება ქიმიურ ინდუსტრიაში, როგორც შესანიშნავი გამხსნელი და ქიმიური რეაგენტი, რომელიც ასინთეზებს სხვა ნივთიერებებს, მაგალითად, აცეტონს.
ტექნიკური ძმრის ესენცია ხშირად გამოიყენება მედიცინაში (მაგალითად, ასპირინი), რბილობი და ქაღალდი (შეღებვისა და ბეჭდვისას), საღებავებსა და ლაქებში, ტექსტილის პარფიუმერიაში, ტყავის და სხვა სამრეწველო დარგებში. იგი გამოიყენება სურნელოვანი ნივთიერებების შერწყმისთვის, ჰერბიციდების წარმოებისთვის და აცეტატური (სინთეზური) ბოჭკოების შესაქმნელად.
ძმარმჟავას მნიშვნელობა სამედიცინო და ფარმაცევტული ინდუსტრიაასევე შესანიშნავია. ეს ნივთიერება არის მთელი რიგი მედიკამენტების განუყოფელი კომპონენტი და წამლებიროგორიცაა ტყვიის და ალუმინის აცეტატის მარილები, აცეტილსალიცილის მჟავა. კომბინაციაში, ისინი გამოიყენება მრავალი დაავადების სამკურნალოდ ანთებითი პროცესებიდა სხვადასხვა დაავადებებიძირითადად პედიკულოზი, ალკოჰოლური მოწამვლა, ლიქენი, რადიკულიტი, პოლიართრიტი და სხვ.
ძმრის ესენცია, ასევე გამხსნელი 646, ფასირომელიც ასევე პატარაა, მისი ყიდვა შეგიძლიათ საყოფაცხოვრებო საქონლის თითქმის ნებისმიერ მაღაზიაში გამონაკლისის გარეშე. ასევე შეგიძლიათ სწრაფად შეუკვეთოთ და შეიძინოთ იგი ინტერნეტის საშუალებით. ღირებულება უფრო იაფი იქნება. ეს განსაკუთრებით სასარგებლოა მათთვის, ვინც მუშაობს ინდუსტრიაში, სადაც საჭიროა მნიშვნელოვანი მოცულობები და სადაც ძმარმჟავა, ისევე როგორც სხვა ქიმიური გამხსნელები, იყიდება მრავალ ლიტრიან ბოთლში და კასრში. ამიტომ, უმჯობესია შეიძინოთ იგი მომწოდებლებისგან, რომლებმაც უკვე დაამტკიცეს საკუთარი თავი და საქონელი ამ ბაზარზე.
ნანახია: 11857 ჯერ
ძმარმჟავა (ძმარმჟავა, ეთანომჟავა, E260) არის სუსტი, შემზღუდველი მონობაზური კარბოქსილის მჟავა.
ძმარმჟავა არის უფერო სითხე დამახასიათებელი მძაფრი სუნით და მჟავე გემოთი. ჰიგიროსკოპიული. წყალში შეუზღუდავად ხსნადი. ქიმიური ფორმულა CH3COOH.
ძმარმჟავას 70-80%-იან წყალხსნარს ძმრის ესენცია ეწოდება, 3-6%-ს კი ძმარი. ძმარმჟავას წყალხსნარი ფართოდ გამოიყენება კვების მრეწველობაში და საყოფაცხოვრებო სამზარეულოში, ასევე საკონსერვო წარმოებაში.
ყურძნის მშრალი ღვინოების ბუნებრივი დამჟავების და სპირტებისა და ნახშირწყლების დუღილის პროდუქტი. მონაწილეობს ორგანიზმში მეტაბოლიზმში. ფართოდ გამოიყენება კონსერვების, მარინადების, ვინეგრეტების დასამზადებლად.
ძმარმჟავა გამოიყენება სამკურნალო და არომატული ნივთიერებების მისაღებად, როგორც გამხსნელი (მაგალითად, ცელულოზის აცეტატის, აცეტონის წარმოებაში). გამოიყენება ბეჭდვისა და შეღებვისას.
ძმარმჟავას მარილებს და ეთერებს აცეტატები ეწოდება.
საკვები დანამატი E260 ყველასთვის ცნობილია, როგორც ძმარმჟავა ან ძმარი. დანამატი E260 გამოიყენება კვების მრეწველობაში, როგორც მჟავიანობის რეგულატორი. ძირითადად, ძმარმჟავას იყენებენ წყალხსნარების სახით 3-9% (ძმარი) და 70-80% (ძმარვის ესენცია) პროპორციით. დანამატს E260 აქვს დამახასიათებელი მკვეთრი სუნი. წყალხსნარებში მჟავიანობის რეგულატორი E260 საკმაოდ სუსტი მჟავაა. მისი სუფთა სახით ძმარმჟავა არის უფერო, კაუსტიკური სითხე, რომელიც შთანთქავს ტენიანობას გარემოდა გაყინვა უკვე 16,5 ° C ტემპერატურაზე მყარი უფერო კრისტალების წარმოქმნით. ძმარმჟავას ქიმიური ფორმულა არის C 2 H 4 O 2 .
ძმარი ცნობილია ათასობით წლის განმავლობაში, როგორც ლუდის ან ღვინის ბუნებრივი დუღილის პროდუქტი. 1847 წელს გერმანელმა ქიმიკოსმა ჰერმან კოლბემ პირველად მოახდინა ძმარმჟავას სინთეზირება ლაბორატორიაში. ახლა მსოფლიოში, ძმარმჟავას მთლიანი წარმოების მხოლოდ 10% მოიპოვება ბუნებრივი მეთოდებით. მაგრამ დუღილის ბუნებრივი მეთოდი ჯერ კიდევ მნიშვნელოვანია, რადგან ბევრ ქვეყანას აქვს კანონები, რომლებიც მოითხოვს მხოლოდ ბიოლოგიურად დაფუძნებულ ძმარმჟავას გამოყენებას კვების მრეწველობაში. E260 დანამატის ბიოქიმიური წარმოებისას გამოიყენება ზოგიერთი ბაქტერიის ეთანოლის (ალკოჰოლის) დაჟანგვის უნარი. ეს მეთოდიცნობილია როგორც ძმარმჟავას დუღილი. E260 დანამატის წარმოებისთვის ნედლეულად გამოიყენება ფერმენტირებული წვენები, ღვინო ან ალკოჰოლის ხსნარი წყალში. ასევე არსებობს ძმარმჟავას სინთეზირების მრავალი სამრეწველო მეთოდი. მათგან ყველაზე პოპულარული, რომელიც მსოფლიოში ძმარმჟავას სინთეზის ნახევარზე მეტს შეადგენს, არის მეთანოლის კარბონილირება კატალიზატორების თანდასწრებით. ამ რეაქციის საწყისი კომპონენტებია მეთანოლი (CH 3 OH) და ნახშირბადის მონოქსიდი (CO).
ძმარმჟავა აუცილებელია მუშაობისთვის ადამიანის სხეული. მისი წარმოებულები ხელს უწყობენ ორგანიზმში ნახშირწყლების და ცხიმების დაშლას, რომლებიც ორგანიზმში საკვებით შედიან. ძმარმჟავა გამოიყოფა გარკვეული ტიპის ბაქტერიების სასიცოცხლო აქტივობის დროს, კერძოდ Clostridium acetobutylicumდა გვარის ბაქტერიები აცეტობაქტერი. ეს ბაქტერიები ყველგან გვხვდება წყალში, ნიადაგში, საკვებში და ბუნებრივადშევიდეს ადამიანის სხეულში.
E260 დანამატის ტოქსიკური მოქმედება ადამიანის სხეულზე დამოკიდებულია ძმარმჟავას წყალთან განზავების ხარისხზე. ხსნარები, რომლებშიც ძმარმჟავას კონცენტრაცია 30%-ზე მეტია, ჯანმრთელობისა და სიცოცხლისთვის სახიფათოა. მაღალი კონცენტრირებული ძმარმჟავა კანთან და ლორწოვან გარსებთან კონტაქტში შეიძლება გამოიწვიოს მძიმე ქიმიური დამწვრობა.
კვების მრეწველობაში E260 დანამატი გამოიყენება საკონდიტრო ნაწარმის საცხობი, ბოსტნეულის დასაკონსერვებლად, მაიონეზისა და სხვა საკვები პროდუქტების დასამზადებლად.
მჟავიანობის რეგულატორი E260 დამტკიცებულია გამოსაყენებლად საკვები პროდუქტებიყველა ქვეყანაში, როგორც ადამიანის ჯანმრთელობისთვის უსაფრთხო დანამატი.
ძმარმჟავა ასევე გამოიყენება:
- ყოველდღიურ ცხოვრებაში (სასწორის ამოღება ქვაბებიდან, ზედაპირების მოვლა);
- ქიმიურ მრეწველობაში (როგორც გამხსნელი და ქიმიური აგენტი);
- მედიცინაში (წამლების მიღება);
- სხვა ინდუსტრიებში.
საკვების კონსერვანტი E260 ძმარმჟავა კარგად არის ცნობილი ყველა ადამიანისთვის, ვინც დაინტერესებულია გასტრონომიის ხელოვნებით. ეს პროდუქტი არის ყურძნის ღვინოების ბუნებრივ პირობებში დამჟავების შედეგი, რომლის დროსაც ხდება ალკოჰოლისა და ნახშირწყლების დუღილი. გარდა ამისა, ცნობილია, რომ ძმარმჟავა უშუალოდ მონაწილეობს ადამიანის ორგანიზმში მეტაბოლურ პროცესებში.
ძმარმჟავას აქვს ძლიერი სუნი, მაგრამ სუფთა ფორმაეს არის სრულიად უფერო სითხე, რომელსაც შეუძლია გარემოდან ტენის შთანთქმა. ამ ნივთიერებას შეუძლია გაყინვა მინუს 16 გრადუს ტემპერატურაზე, რის შედეგადაც წარმოიქმნება გამჭვირვალე კრისტალები.
აღსანიშნავია, რომ ძმარმჟავას 3-6%-იან ხსნარს ძმარი ჰქვია, 70-80 პროცენტით კი ძმრის ესენცია მიიღება. E260 წყალზე დაფუძნებული ხსნარები ფართოდ გამოიყენება არა მხოლოდ კვების მრეწველობაში, არამედ საყოფაცხოვრებო სამზარეულოში. საკვების კონსერვანტის E260 ძმარმჟავას ძირითადი გამოყენება არის მარინადების და დაკონსერვებული საკვების წარმოება.
გარდა ამისა, ეს ნივთიერება აქტიურად ემატება და როდის სამრეწველო წარმოებამთელი რიგი საკონდიტრო ნაწარმი, ასევე მაიონეზი და ბოსტნეულის კონსერვი. ხშირად, საჭიროების შემთხვევაში, საკვების კონსერვანტი E260 ძმარმჟავა შეიძლება გამოყენებულ იქნას როგორც სადეზინფექციო და სადეზინფექციო საშუალება.
თუმცა, საკვების წარმოების არეალი არ არის ერთადერთი ზონა საკვების კონსერვანტის E260 გამოყენებისთვის. ამრიგად, იგი ფართოდ გამოიყენება ქიმიურ წარმოებაში ორგანული მინის, აცეტატური ბოჭკოების წარმოებაში, ასევე ეთერებისა და მედიკამენტების წარმოებაში.
სხვათა შორის, ფარმაკოლოგიაში ფართოდ გამოიყენება ეგრეთ წოდებული ძმარმჟავას ეთერი, რომელიც უფრო ცნობილია ადამიანისთვის აცეტილსალიცილის მჟავას ან ასპირინის სახელწოდებით. როგორც გამხსნელი, ძმარმჟავა ასევე ეხმარება ადამიანებს რიგ შემთხვევებში და მისი შემადგენლობიდან გამოყოფილი მარილები წარმატებით გამოიყენება მცენარეთა მავნებლებთან ბრძოლაში.
საკვების კონსერვანტის საზიანო E260 ძმარმჟავა
საკვების კონსერვანტის E260 ძმარმჟავას ზიანი ადამიანისთვის განსაკუთრებით აშკარაა, როდესაც ეს ნივთიერება მოიხმარება მაღალი კონცენტრაციით, რადგან ამ ფორმით ის ძალიან ტოქსიკურია. სხვათა შორის, მჟავა ტოქსიკურობის ხარისხი პირდაპირ დამოკიდებულია იმაზე, თუ რამდენად იყო იგი წყლით განზავებული. ხსნარები, რომელთა კონცენტრაცია აღემატება 30 პროცენტს, ჯანმრთელობისთვის ყველაზე საშიშად ითვლება. როდესაც ლორწოვანი გარსები ან კანი შედის კონცენტრირებულ ძმარმჟავასთან კონტაქტში, ხდება მძიმე ქიმიური დამწვრობა.
სურსათის კონსერვანტი E260 ძმარმჟავა დამტკიცებულია კვების მრეწველობაში გამოსაყენებლად მსოფლიოს ყველა ქვეყანაში, რადგან არ ითვლება ჯანმრთელობისთვის საშიშად. ერთადერთი, რასაც ექსპერტები გვირჩევენ, რათა თავიდან იქნას აცილებული საკვების კონსერვანტის E260 ძმარმჟავას შესაძლო ზიანი, არის ამ ნივთიერების პროდუქტების შეზღუდვა ღვიძლისა და კუჭ-ნაწლავის დაავადებების მქონე ადამიანების შემადგენლობაში. ასეთი პროდუქტების მიცემა არ არის რეკომენდებული 6-7 წლამდე ბავშვებისთვის.
ძმარმჟავა
ღვინის აქროლადი მჟავები არის მონობაზური ცხიმოვანი მჟავები, რომელთა შემადგენლობაში შედის ზოგადი ფორმულა.
ეს არის ფორმული, ძმარმჟავა, პროპიონის, ბუტირის, ვალერიკის, კაპრილის და სხვა უმაღლესი ცხიმოვანი მჟავები. აქროლად მჟავებს შორის მთავარია რაოდენობრივად და ღირებულებით ძმარმჟავა. ღვინოების აქროლადი მჟავიანობის ყველა ანალიტიკური განსაზღვრა ხდება ძმარმჟავას მიხედვით.
ღვინის აქროლადი მჟავებიალკოჰოლური დუღილის ქვეპროდუქტებია. დუღილის დროს, აქროლადი მჟავების ყველაზე მცირე რაოდენობა წარმოიქმნება ტემპერატურის დიაპაზონში 15 ºС-დან 25 ºС-მდე. უფრო მაღალი და მეტი დაბალი ტემპერატურადუღილი ხელს უწყობს აქროლადი მჟავების უფრო დიდი მასის წარმოქმნას. აერობული დუღილის პირობებში წარმოიქმნება ნაკლებად არასტაბილური პირობები.
აქროლადი მჟავები გამოხდილია ორთქლით. ეს თვისება საფუძვლად უდევს მათი რაოდენობრივი განსაზღვრის ყველა მეთოდს.
აქროლადი მჟავების მარილები ადვილად ხსნადია წყალში და ალკოჰოლში. სასურველია აქროლადი მჟავების ეთერები მცირე რაოდენობით შემადგენელი ნაწილიაღვინისა და კონიაკის თაიგულები.
ძმარმჟავა(CH3COOH) ცნობილია უძველესი დროიდან. მის მჟავას რადიკალს ე.წ აცეტილი"მჟავას ლათინური აღნიშვნიდან - « მჟავა აცეტიკუმი» . მისი სუფთა სახით, უწყლო ძმარმჟავა არის უფერო სითხე მძაფრი სუნით, რომელიც მყარდება კრისტალურ მასად 16°C-ზე დაბალ ტემპერატურაზე. ძმარმჟავას დუღილის წერტილი არის + 118,5 ºС.
ინჟინერიაში გამოიყენება როგორც ძმარმჟავა, ასევე მისი მარილები. მარილები გამოიყენება ტექსტილის, ქიმიურ, ტყავის და რეზინის მრეწველობაში. თავად ძმარმჟავა გამოიყენება აცეტონის, ცელულოზის აცეტატების, არომატული ნივთიერებების მოსამზადებლად, გამოიყენება მედიცინაში, კვების მრეწველობაში და გამოიყენება მარინადების მოსამზადებლად.
ტყვიის ძმარი (CH3 COOH) 2Pb· Pb(ოჰ)2 გამოიყენება თეთრის წარმოებაში და ში ქიმიური ანალიზიფენოლური ნივთიერებების დალექვისთვის.
ძმარმჟავას საფუძველზე ამზადებენ ეგრეთ წოდებულ სუფრის ძმარს, რომელიც ფართოდ გამოიყენება მცირე რაოდენობით სხვადასხვა კერძების არომატიზებისთვის. კულინარიაში დიდი მოთხოვნაა ღვინისგან მიღებული ნატურალური ღვინის ძმარი.
სუფრის ღვინის ძმრის მოსამზადებლად წყალში გაზავებულ ღვინოს ოდნავ ამჟავებენ ძმრით და ათავსებენ ბრტყელ ჭურჭელში ან ღია კასრებში. ძმარმჟავას ბაქტერიების ფილმი გამოიყენება სითხის ზედაპირზე. ფართო საჰაერო წვდომა (აერაცია), ცხელებადა სულფიტაციის სრული არარსებობა ხელს უწყობს ძმარმჟავას ბაქტერიების სწრაფ განვითარებას და ეთილის სპირტის სწრაფ გარდაქმნას ძმარმჟავად.
ძმარმჟავა არის ალკოჰოლური დუღილის სავალდებულო ქვეპროდუქტი და შეადგენს აქროლადი მჟავების ძირითად ნაწილს.
ღვინოში აქროლადი მჟავების შემცველობის მატება აიხსნება მათი გაჩენით ღვინის მრავალ დაავადებაში და სხვადასხვა აქტივობის შედეგად. პათოგენური ბაქტერიები. ყველაზე საშიში და ამავდროულად ყველაზე გავრცელებული ღვინის დაავადებაა ძმარი მჟავე.ამ დაავადებით ეთანოლიგვარი ძმარმჟავას მოქმედებით (Bact. aceti და სხვ.) იჟანგება ძმარმჟავად:
დროული შევსება, ღვინის მასალების შენახვა 10-12 ºС ტემპერატურაზე, ზომიერი სულფიტაცია ხელს უშლის ღვინოში ძმარმჟავას წარმოქმნას. ძმარმჟავა ბაქტერიები არიან აერობები და ძალიან მგრძნობიარენი არიან გოგირდმჟავას მიმართ, რაც ზღუდავს ჟანგბადის წვდომას ღვინოზე.
ძმარმჟავას მჟავიანობით დაავადებული ღვინოების გამოსასწორებლად, ღვინის ზედაპირზე შეიძლება დამუშავდეს შერის ფილმი. ღვინოზე განვითარებული შერის საფუარი მნიშვნელოვნად ამცირებს აქროლადი მჟავების შემცველობას. სუფრის ღვინოები აქროლადი მჟავების მაღალი (4 გ/დმ3-ზე მეტი) შემცველობით, ძმარმჟავას ფენის ამოღების შემდეგ პასტერიზებულია ძმარმჟავას ბაქტერიების მოსაკლავად, ალკოჰოლიზირებული და გამოიყენება ჩვეულებრივი ძლიერი ღვინოების ნარევებში. ძმარმჟავა ბაქტერიები ასევე შეიძლება განადგურდეს სულფიტაციით მინიმუმ 100 მგ/დმ3 დოზით ბენტონიტით და ღვინის ფილტრაციით დაუყონებლივ დამუშავებით.
ღვინის აქროლადი მჟავები - 3.0 5-დან 3 ხმის საფუძველზე
კოლბის ნამუშევრებით, ძმარმჟავას და ამავდროულად ყველა სხვა ორგანული მჟავის სტრუქტურა საბოლოოდ გაირკვა და შემდგომი ქიმიკოსების როლი მხოლოდ დაყოფამდე შემცირდა - თეორიული მოსაზრებებისა და ჟერარდის ავტორიტეტის გამო, კოლბის ფორმულები ნახევრად. და სტრუქტურული შეხედულებების ენაზე თარგმნა, რის გამოც ფორმულა C2H6.C2O4H2 გადაიქცა CH3.CO(OH-ად).
2. ძმარმჟავას თვისებები
კარბოქსილის მჟავები - ორგანული ნაერთები, რომლებიც შეიცავს ერთ ან მეტ კარბოქსილის ჯგუფს -COOH, დაკავშირებული ნახშირწყალბადის რადიკალთან.
მჟავა თვისებები კარბოქსილის მჟავებიგანპირობებულია ელექტრონის სიმკვრივის კარბონილის ჟანგბადზე გადანაცვლებით და შედეგად მიღებული დამატებითი (ალკოჰოლებთან შედარებით) О–Н ბმის პოლარიზაციასთან. წყალხსნარში კარბოქსილის მჟავები იშლება იონებად:მატებასთან ერთად მოლეკულური წონაწყალში მჟავების ხსნადობა მცირდება. კარბოქსილის ჯგუფების რაოდენობის მიხედვით მჟავები იყოფა ერთბაზიან (მონოკარბოქსილურ) და პოლიბაზურ (დიკარბოქსილის, ტრიკარბოქსილის და სხვ.).
ნახშირწყალბადის რადიკალის ბუნების მიხედვით განასხვავებენ გაჯერებულ, უჯერი და არომატულ მჟავებს.
მჟავების სისტემატური სახელები მოცემულია შესაბამისი ნახშირწყალბადის სახელით, სუფიქსის დამატებით. -ოვაიადა სიტყვები მჟავა. ხშირად გამოიყენება ტრივიალური სახელებიც.
ზოგიერთი გაჯერებული მონობაზის მჟავა
|
ფორმულა |
სახელი |
|
|
სისტემატური |
ტრივიალური |
|
|
მეთანი |
ფორმული |
|
|
ეთანი |
ძმარმჟავა |
|
|
პროპანი |
პროპიონური |
|
|
ბუტანი |
ზეთოვანი |
|
|
პენტანი |
ვალერიანი |
|
|
ჰექსანი |
კაპრონი |
|
|
პენტადეკანური |
პალმიტური |
|
|
ჰეპტადეკანური |
სტეარიული |
|
კარბოქსილის მჟავები ძალიან რეაქტიულია. ისინი რეაგირებენ სხვადასხვა ნივთიერებებთან და ქმნიან სხვადასხვა ნაერთებს, რომელთა შორის დიდი მნიშვნელობა აქვს ფუნქციური წარმოებულები, ე.ი. კარბოქსილის ჯგუფში რეაქციების შედეგად მიღებული ნაერთები.
2.1 მარილების წარმოქმნა ა) ლითონებთან ურთიერთობისას:
2RCOOH + Mg® (RCOO) 2Mg + H2
ბ) ლითონის ჰიდროქსიდებთან რეაქციებში:
2RCOOH + NaOH ® RCOONa + H2O
კარბოქსილის მჟავების ნაცვლად, მათი მჟავა ჰალოიდები უფრო ხშირად გამოიყენება: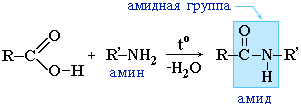 |
ამიდები ბუნებაში მნიშვნელოვან როლს ასრულებენ. ბუნებრივი პეპტიდების და ცილების მოლეკულები აგებულია ა-ამინომჟავებისგან ამიდური ჯგუფების - პეპტიდური ბმების მონაწილეობით.
ძმარმჟავა (ეთანოინის მჟავა).
ფორმულა: CH 3 - COOH; გამჭვირვალე უფერო სითხე მძაფრი სუნით; დნობის წერტილის ქვემოთ (mp 16,6 გრადუსი C) ყინულის მსგავსი მასა (ამიტომ, კონცენტრირებულ ძმარმჟავას ასევე უწოდებენ მყინვარ ძმარმჟავას). ხსნადი წყალში, ეთანოლში.
ცხრილი 1. ძმარმჟავას ფიზიკური თვისებები
| სახელი | მჟავის ფორმულა |
ხსნადობა (გ/100მლ H2O;25°C) | კა (25°C-ზე) |
|||||
|
მისი მარილები (ესტერები) |
||||||||
|
ძმარმჟავა |
ეთანი | |||||||
მსგავსი სტატიები
-
ინგლისური - საათი, დრო
ყველას, ვისაც აინტერესებს ინგლისური ენის შესწავლა, მოუწია უცნაურ აღნიშვნებს გვ. მ. და ა. მ , და საერთოდ, სადაც დროა ნახსენები, რატომღაც მხოლოდ 12 საათიანი ფორმატი გამოიყენება. ალბათ ჩვენთვის მცხოვრები...
-
"ალქიმია ქაღალდზე": რეცეპტები
Doodle Alchemy ან Alchemy ქაღალდზე Android-ისთვის არის საინტერესო თავსატეხი ლამაზი გრაფიკით და ეფექტებით. ისწავლეთ როგორ ითამაშოთ ეს საოცარი თამაში და იპოვეთ ელემენტების კომბინაციები, რათა დაასრულოთ ალქიმია ქაღალდზე. Თამაში...
-
თამაშის ავარია Batman: Arkham City?
თუ თქვენ წინაშე აღმოჩნდებით, რომ Batman: Arkham City ანელებს, ავარია, Batman: Arkham City არ დაიწყება, Batman: Arkham City არ დაინსტალირდება, არ არის კონტროლი Batman: Arkham City, არ არის ხმა, გამოდის შეცდომები. ზევით, ბეტმენში:...
-
როგორ მოვიშოროთ ადამიანი სათამაშო აპარატებიდან როგორ მოვიშოროთ ადამიანი აზარტული თამაშებისგან
მოსკოვის Rehab Family კლინიკის ფსიქოთერაპევტთან და აზარტულ თამაშებზე დამოკიდებულების მკურნალობის სპეციალისტთან რომან გერასიმოვთან ერთად, რეიტინგის ბუკმეიკერებმა სპორტულ ფსონებში მოთამაშეს გზა გაუკვლიეს - დამოკიდებულების ჩამოყალიბებიდან ექიმთან ვიზიტამდე,...
-
Rebuses გასართობი თავსატეხები თავსატეხები გამოცანები
თამაში "RIDDLES Charades Rebuses": პასუხი განყოფილებაში "RIDDLES" დონე 1 და 2 ● არც თაგვი, არც ჩიტი - ის ხარობს ტყეში, ცხოვრობს ხეებზე და ღრღნის თხილს. ● სამი თვალი - სამი ბრძანება, წითელი - ყველაზე საშიში. დონე 3 და 4 ● ორი ანტენა თითო...
-
შხამისთვის თანხების მიღების პირობები
რამდენი თანხა მიდის SBERBANK-ის ბარათის ანგარიშზე გადახდის ოპერაციების მნიშვნელოვანი პარამეტრებია სახსრების დაკრედიტების პირობები და ტარიფები. ეს კრიტერიუმები, პირველ რიგში, დამოკიდებულია თარგმანის არჩეულ მეთოდზე. რა პირობებია ანგარიშებს შორის თანხის გადარიცხვისთვის
