კარბოქსილის მჟავა. უჯერი კარბოქსილის მჟავები
ლექცია #10
კარბოქსილის მჟავები
კარბოქსილის მჟავას მოლეკულა შეიცავს კარბოქსილის ჯგუფი
(კარბოქსი). ნაერთში კარბოქსილი შეიძლება დაუკავშირდეს ალკილის ჯგუფს (ლიმიტი კარბოქსილის მჟავები) ან ალკენის ნარჩენი (უჯერი კარბოქსილის მჟავები). გარდა ამისა, კარბოქსილის მჟავა შეიძლება შეიცავდეს რამდენიმე კარბოქსილს. დამოკიდებულია მათ რაოდენობაზე საბაზისომჟავები.
შეზღუდეთ მონობაზური მჟავები.
მჟავების ტრივიალური სახელები ასახავს მათ ბუნებრივ წყაროს. მაგალითად, სამი მჟავა 6,8,10-დანნახშირბადის ატომები იზოლირებული იყო თხის ცხიმისგან კარაქის ჰიდროლიზის პროდუქტებიდა დასახელებულია შესაბამისად კაპროული, კაპრილის და კაპრინის მჟავები (ლათინურიდან კაპერი- თხა).
მჟავები და მათი სახელები ტრივიალური და სისტემატური ნომენკლატურის მიხედვით
სისტემატური ნომენკლატურის მიხედვით, კარბოქსილის მჟავამ მიიღო თავისი სახელი ნახშირბადის ატომების ყველაზე გრძელი ჯაჭვის მქონე შესაბამისი ნახშირწყალბადის სახელიდან. ჯაჭვი დანომრილია და ათვლა იწყება კარბოქსილის ნახშირბადიდან. სახელში მითითებულია შემცვლელი რადიკალები და მათი პოზიცია.
უნდა აღინიშნოს, რომ ზოგიერთი მჟავა მოლეკულაში ნახშირბადის დიდი რაოდენობით კლასიფიცირებულია, როგორც უმაღლესი ცხიმოვანი მჟავები (მაგალითად, პალმიტური და სტეარიული). ეს სახელი აერთიანებს ბუნებრივ სწორ ჯაჭვის მჟავებს, რომლებიც ეთერების სახით მცენარეებისა და ცხოველების ცხიმების, ცვილებისა და ზეთების ნაწილია.
როდესაც ჰიდროქსილის ჯგუფი ამოღებულია კარბოქსილიდან, მიიღება მონოვალენტური მჟავის ნარჩენები ან აცილები,და ზე წყალბადის გაყოფა - ე. წ აცილატიჯგუფები
H-CO- ფორმილ H-COO- ფორმატი
CH 3 CO- აცეტილ CH 3 COO- აცეტატი
CH 3 CH 2 CO- პროპიონილ CH 3 CH 2 COO- პროპიონატი
CH 3 CH 2 CH 2 CO-ბუტირილ CH 3 CH 2 CH 2 COO-ბუტირატი
CH 3 CH 2 CH 2 CH 2 CO-ვალერილ CH 3 CH 2 CH 2 CH 2 COO- ვალერატი
კარბოქსილის მჟავების წარმოებულების სახელები დაკავშირებულია თავად მჟავების სახელებთან. როგორ არის შედგენილი მჟავების წარმოებულების სახელები, ჩანს ქვემოთ მოცემული მაგალითებიდან.
CH 3 COOH CH 3 COONa CH 3 COCl
ძმარმჟავანატრიუმის აცეტატი აცეტილ ქლორიდი
ეთანი ახალი მჟავა ეთანი შვრიის ნატრიუმის ეთანი ზეთი ქლორიდი
(CH 3 CO) 2 O CH 3 CH 2 OSOCH 3 CH 3 CONH 2
ძმარმჟავას ანჰიდრიდი ეთილის აცეტატი აცეტამიდი
ეთანის ანჰიდრიდი ეთილის ეთანი შვრიის ეთანამიდი
CH 3 CONHCH 3 CH 3 CN
N-მეთილაქეტამიდი აცეტონიტრილი
N-მეთილეთანამიდი ეთანენიტრილი
1.2. მიღების მეთოდები.
ეს არის რეაქციები დაჟანგვაალკანები, ალკენები და ალკინები, პირველადი სპირტები და ალდეჰიდები, ჰიდროლიზი ჰალოგენის წარმოებულები სამი ჰალოგენით ერთში ნახშირბადის და კარბოქსილის მჟავების წარმოებულები: ნიტრილები, კომპლექსი ეთერები, ორთოესტერები, ანჰიდრიდები, მჟავა ჰალოიდები და ამიდები. და ა.შ.
1.2. ფიზიკური თვისებები.
კარბოქსილის მჟავების ერთ-ერთი საოცარი თვისებაა მათი სითბომდუღარე. შედარებისთვის, ქვემოთ მოცემულია ზოგიერთი ნაერთების დუღილის წერტილი (0 C)
აცეტალდეჰიდი 21
ეთილის აცეტატი 77
ძმარმჟავა 118
მჟავებს უფრო მაღალი დუღილის წერტილი აქვთ ვიდრე ალკოჰოლს. ამის ახსნა უკვე რთულია მხოლოდ მჟავას მოლეკულებს შორის წყალბადის ბმების წარმოქმნით. კარბოქსილის მჟავების მოლეკულებს შეუძლიათ ერთმანეთთან დაკავშირება არა ერთი, არამედ ორი წყალბადის ბმით.
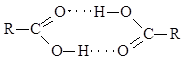
შედეგად, ორი მჟავის მოლეკულა იმდენად ძლიერად არის შეკრული, რომ ისინი დიმერის სახით არსებობენ არა მხოლოდ თხევად ან მყარ ფაზაში, არამედ ორთქლებშიც კი.
წყალში ქვედა მჟავების მაღალი ხსნადობა ასევე აიხსნება წყალბადის ბმების წარმოქმნით, რომელშიც შედის მჟავა და გამხსნელი მოლეკულები. ამ შემთხვევაში, წყლის მოლეკულები მოთავსებულია კარბოქსილის მჟავას მოლეკულებს შორის
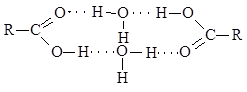
ქიმიური თვისებები.
კარბოქსილის მჟავების ქიმიური თვისებები განპირობებულია მათ მოლეკულაში არსებობით კარბოქსილის ჯგუფი, რომელიც არის კომბინაცია კარბონილის და ჰიდროქსილის ჯგუფები. ამავდროულად, კარბოქსილის მჟავების ქიმიური თვისებები არ არის მხოლოდ ალკოჰოლებისა და კარბონილის ნაერთების თანდაყოლილი თვისებების ერთობლიობა, ის ასევე არის ახალი ხარისხი.
1.3.1. მჟავიანობა. მარილის ფორმირება.
მონობაზური გაჯერებული კარბოქსილის მჟავები, მართალია სუსტი, მაგრამ "ნამდვილი" მჟავებია - მათი აღმოჩენა შესაძლებელია ლაკმუსის ქაღალდის გამოყენებით..
როგორც მჟავები, კარბოქსილის მჟავები ემსახურებიან პროტონების წყაროს, ამიტომ მათ შეუძლიათ იონიზაცია. წყალხსნარში მჟავა იონირდება განტოლების მიხედვით
წონასწორობა დამყარებულია მჟავასა და კარბოქსილატ ანიონსა და პროტონს შორის. წონასწორობის მუდმივი კ ა(მჟავიანობის მუდმივი, მჟავა) შებოჭვის კონცენტრაცია, გამოითვლება განტოლების საფუძველზე
მჟავე ვარ?
ეთანოლისა და ძმარმჟავას იონიზაცია მიმდინარეობს, შესაბამისად, ალკოჰოლური და კარბოქსილატური ანიონების წარმოქმნით.
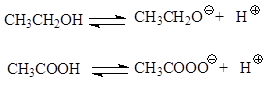
კარბოქსილის მჟავებს შორის ყველაზე ძლიერია ჭიანჭველა მჟავა. კარბოქსილის ჯგუფში წყალბადის ნაცვლად მეთილის ელექტრონის შემომწირველი რადიკალის გამოჩენა იწვევს მჟავიანობის შემცირებას თითქმის ათჯერ. მეთილის ჯგუფში წყალბადის ატომების ჰალოგენებით ჩანაცვლების შემთხვევაში წარმოიქმნება ელექტრონის ამომყვანი შემცვლელი, რომელიც აძლიერებს მჟავიანობას. მჟავიანობის ცვლილების თანმიმდევრობა (10 5 კ ა) რიგი მჟავები ადასტურებს ნათქვამს
CH 3 COOH 1.75
ClCH 2 COOH 136
Cl2CHCOOH 5530
Cl 3 COOH 23200
CH 3 CH 2 CH 2 COOH 1.52
CH 3 CH 2 CHClCOOH 139
CH 3 CHClCH 2 COOH 8.9
CH 2 ClCH 2 CH 2 COOH 2.96
ასე რომ, კარბოქსილის მჟავები სუსტი მჟავებია და ტუტეებთან რეაქციაში იძლევა მარილებს
ტუტე ლითონის მარილების პიროლიზის დროს კაუსტიკური ტუტეების მონაწილეობით ხდება დეკარბოქსილაცია და ალკანების წარმოქმნა. კალციუმის ან ბარიუმის მარილების პიროლიზი ტუტეების არარსებობის შემთხვევაში იწვევს ალდეჰიდებს და კეტონებს (პირია რეაქცია). კარბოქსილის მჟავების ნატრიუმის მარილების ელექტროლიზი შესაძლებელს ხდის ნაერთების მიღებას, მაგალითად, ალკანებს, რომლებიც შეიცავს ორჯერ მეტ შემცვლელს კარბოქსილის მჟავაზე (კოლბის რეაქცია). კარბოქსილის მჟავების მარილების განხილვისას არ შეიძლება არ აღინიშნოს უმაღლესი ცხიმოვანი მჟავების (ნატრიუმის სტეარატი) ტუტე ლითონის მარილების მუდმივი მნიშვნელობა, როგორც სარეცხი საშუალებები.
1.3.2. აცილჰალოგენების წარმოქმნა.
კარბოქსილის მჟავების მჟავა ჰალოიდები.
კარბოქსილის მჟავების მჟავა ჰალორიდები, ყველაზე ხშირად მჟავა ქლორიდები, ადვილად მიიღება მჟავების ფოსფორის ტრი- ან პენტაქლორიდთან, თიონილ ქლორიდთან და ფოსგენთან რეაქციით.
კარბოქსილის მჟავების ყველა წარმოებულებიდან, აცილჰალოგენები ავლენენ უდიდეს რეაქტიულობას. ეს გამოწვეულია ამ ნაერთებში ჰალოგენის მაღალი მობილურობით.
მჟავა ჰალოგენების რეაქციები მიმდინარეობს ნუკლეოფილური ჰალოგენის შემცვლელი რეაქციების სახით და იწვევს სხვა მჟავას წარმოებულებს.

ყველა ამ რეაქციაში მოლეკულაში შეჰყავთ მჟავე ნარჩენი - აცილიასე რომ, მათი საერთო სახელია აცილაციის რეაქციები. კარბოქსილის მჟავას ჰალოიდები საუკეთესო აცილირებადი აგენტია.
რეაქცია იწყება ნუკლეოფილური დანამატით კარბონილის ჯგუფს მჟავა ჰალოიდში, როგორც ალდეჰიდების და კეტონების შემთხვევაში
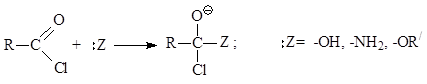
ჰალოაცილში ნუკლეოფილის დამატების შუალედური პროდუქტი შლის ჰალოგენის ატომს, წარმოქმნის კარბონილის ჯგუფს და იძლევა შემცვლელ პროდუქტს.

ნუკლეოფილური ჩანაცვლება ჰალოაცილებში აშკარაა. სინამდვილეში, რეაქცია ხდება როგორც "მიმაგრება - გაყოფა". მჟავა ჰალოგენებში ჰალოგენის ატომი იცვლება არა იმიტომ, რომ ის მობილურია, არამედ იმიტომ, რომ ის არის ფუნქციური ჯგუფის ნაწილი, რომელსაც შეუძლია დამატების რეაქცია.
1.3.3. ანჰიდრიდების წარმოქმნა.
ანჰიდრიდების მომზადების საერთო მეთოდია მჟავა მარილების რეაქცია მჟავა ჰალოგენებთან
კარბოქსილის მჟავების რეაქცია ჰალოაცილებთან პირიდინის თანდასწრებით ასევე იწვევს ანჰიდრიდებს.
ბოლოს აღვნიშნავთ, რომ ანჰიდრიდები ასევე მიიღება კარბოქსილის მჟავებისა და კეტენისგან
მჟავა ანჰიდრიდები, ჰალოაცილების მსგავსად, გამოიყენება აცილირების რეაქციებში. მჟავა ანჰიდრიდები რბილი რეაგენტებია; მათი გამოყენებისას აგრესიული მარილმჟავა არ გამოიყოფა, როგორც ჰალოაცილების გამოყენებისას.
მჟავა ანჰიდრიდებთან აცილებისას, რომელიც მიმდინარეობს ჰალოაცილების მონაწილეობით განხილული რეაქციის მსგავსად, მიიღება კარბოქსილის მჟავების სხვა წარმოებულები.
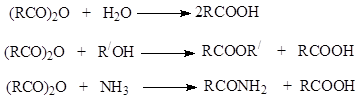
1.3.4. ეთერიფიკაცია. რთული ეთერები.
რეაქცია კარბოქსილის მჟავებსა და ალკოჰოლებს შორის მჟავა კატალიზატორის თანდასწრებით იწვევს ეთერებს, რომელსაც ე.წ. ესტერიფიკაციის რეაქცია
რეაქციის მოცემულ ვარიანტს ჩვეულებრივ უწოდებენ ესტერიფიკაციას ფიშერი(ფიშერი, 1895).
ესტერიფიკაციაზე გავლენას ახდენს სივრცითი ფაქტორები. თუ რეაქციის მონაწილეთა რეაქციის ცენტრთან არის ნაყარი ჯგუფები, მაშინ ესტერიფიკაციის სიჩქარე ნელდება.
ფიშერის ესტერიფიკაცია მიმდინარეობს როგორც ნუკლეოფილური აცილის ჩანაცვლება "დამატება-ელიმინაციის" მექანიზმის მიხედვით.
ალკოჰოლების აცილებისას კარბოქსილის მჟავის ნაცვლად ხშირად გამოიყენება უფრო რეაქტიული ჰალოაცილები და მჟავა ანჰიდრიდები.
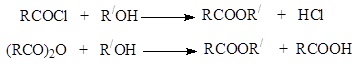
იმ შემთხვევებში, როდესაც ამა თუ იმ მიზეზით, ეთერების სინთეზი აცილირებით რთულია, გამოიყენება სხვა მეთოდები: ჰალოალკილების ჰალოგენის ჩანაცვლება კარბოქსილატური ანიონით კარბოქსილის მჟავების ვერცხლის მარილებით ან მჟავების უშუალო დამატებით აქტიურ ალკენებში. :
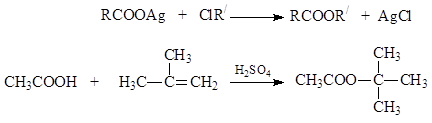
ასევე არსებობს მეთილის ეთერების მიღების მეთოდი კარბოქსილის მჟავების დიაზომეთანთან ეთერის ხსნარში რეაქციით.
ეთერებს შეუძლიათ მრავალი გარდაქმნა.
1.3.4.1. ჰიდროლიზი.
წყალთან ურთიერთობისას ეთერები ჰიდროლიზდება.
ჰიდროლიზის მექანიზმი მიჩნეულია რეაქციის მიმდინარეობად აცილ-ჟანგბადის ბმის გაწყვეტით. ეს დადგინდა ჟანგბადის O 18 იზოტოპის შემცველ წყალთან ერთად ესტერის ჰიდროლიზის ექსპერიმენტების შედეგების საფუძველზე.
აღმოჩნდა, რომ ჰიდროლიზის დროს ჟანგბადის იზოტოპი შედის კარბოქსილის მჟავას შემადგენლობაში. ეს აშკარად მიუთითებს ჰიდროლიზის რეაქციის წარმოქმნაზე ჟანგბად-აცილური ბმის გაწყვეტით.
ესტერიფიკაციისგან განსხვავებით, ეთერების ჰიდროლიზი ასევე კატალიზებულია ბაზებით (საპონიფიკაცია). სტერეოქიმიური კვლევებისა და O 18-ის გამოყენების ექსპერიმენტების შედეგების საფუძველზე დადგინდა, რომ ამ შემთხვევაშიც რეალიზებულია „მიმაგრება-გაწყვეტის“ მექანიზმი, რომელიც მიმდინარეობს აცილ-ჟანგბადის ბმის რღვევით.

მჟავა კატალიზატორი აკატალიზებს როგორც ესტერიფიკაციას, ასევე საპირისპირო რეაქციას, ჰიდროლიზს. მთავარი კატალიზატორი მხოლოდ ჰიდროლიზია. ჩნდება კითხვა, რატომ არ ახდენს ძირითადი კატალიზატორი ესტერიფიკაციის კატალიზებას?
1.3.4.2. ინტერესტერიფიკაცია. როდესაც ესტერი რეაგირებს ჭარბ ალკოჰოლთან მჟავების ან ფუძეების თანდასწრებით, ეთერში ერთი ალკილი იცვლება მეორით. ერთი ეთერიდან მეორე მიიღება, ჩნდება ინტერტერიზაცია
როგორც სხვა მაგალითი, ჩვენ მივუთითებთ ტრანსესტერიფიკაციის გამოყენებას პოლივინილის სპირტის წარმოებისთვის, რომელიც ვერ მიიღება უშუალოდ ვინილის სპირტის პოლიმერიზაციით. მეთანოლთან ტრანსესტერიფიცირებისას პოლიმერი იძლევა სტაბილურ პოლივინილ სპირტსა და მეთილის აცეტატს
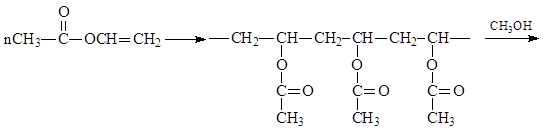
1.3.4.3. რეაქცია გრიგნარდის რეაგენტთან. ეს რეაქცია უკვე ნახსენებია, როგორც მესამეული სპირტების მიღების მეთოდი. იგი მიმდინარეობს ზოგადი სქემის შესაბამისად, როგორც ნუკლეოფილური ჩანაცვლება გრიგნარდის რეაგენტის ალკილის ჯგუფის ნუკლეოფილური დამატების გზით ეთერის კარბონილის ჯგუფის ელექტრონ-დეფიციტურ ნახშირბადში. ამ შემთხვევაში წარმოქმნილ I ანიონს შეუძლია რეაგირება მოახდინოს Mg + Br-თან და წარმოქმნას ალკოჰოლატი II ან სხვაგვარად აღმოფხვრას ალკოქსი ჯგუფი კეტონად გარდაქმნით.

გამორჩეული თვისებამესამეული სპირტების სინთეზი განხილული მეთოდით არის ის, რომ ამ შემთხვევაში სპირტები ორი იდენტური ნახშირწყალბადის ნარჩენებით მიიღება ჰიდროქსილის ჯგუფების ნახშირბადთან.
ფორმატების გამოყენება გრიგნარდის რეაგენტებთან რეაქციაში შესაძლებელს ხდის მეორადი სპირტების მიღებას.
1.3.4.4. ამონოლიზი. ეთერების რეაქცია ამიაკთან ამ შემთხვევაში, გამომავალი ალკოქსი ჯგუფი იცვლება ამინო ჯგუფით და წარმოიქმნება კარბოქსილის მჟავას ამიდი.
1.3.4.5. აღდგენა. ეთერების შემცირების შედეგად, რომელსაც თან ახლავს ჟანგბადისა და მჟავას ნარჩენებს შორის კავშირის გაწყვეტა, მიიღება ორი სპირტი.
შემცირება შეიძლება განხორციელდეს ატომური წყალბადით მეტალის ნატრიუმის და დაბალი დუღილის ალკოჰოლის გამოყენებით (ბუვოტის და ბლანის მეთოდი)
ბოლო დროს რესტავრაცია სასურველია ჩატარდეს ლითიუმის ალუმინის ჰიდრიდით.
ინდუსტრიაში ჰიდროგენოლიზი ყველაზე ხშირად ტარდება კატალიზური ვერსიით მოლეკულური წყალბადით წნევის ქვეშ. კარგად მუშაობდა როგორც კატალიზატორი სპილენძის ქრომიტი(დაახლოებითი შემადგენლობის ოქსიდების ნარევი CuO. CuCr 2 O 4).
1.3.4.6. ესტერის კონდენსაცია. ეთერებს, რომლებსაც აქვთ წყალბადის ატომები კარბოქსილის ჯგუფთან მიმდებარე ნახშირბადთან, ალკოჰოლატების თანდასწრებით, შეუძლიათ შევიდნენ კონდენსაციის რეაქციაში. კლაისენი)
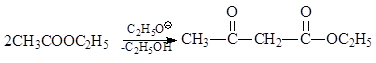
ამ ეთერში მეთილენის ჯგუფის წყალბადის ატომები, რომლებიც მდებარეობს ორ კარბონილს შორის, ხდება ისე მჟავე, რომ შესაძლებელი ხდება აცეტოაცეტატური ეთერის - ეთანოლის გადაადგილება მისი მარილიდან ნატრაცეტოძმარვის ეთერის წარმოქმნით.
1.3.4.7. ეთერები ქმნიან ისეთ მნიშვნელოვან ბუნებრივ პროდუქტებს, როგორიცაა ცხიმები და ზეთები - ეს არის გლიცეროლის ეთერები და გაჯერებული და უჯერი უჯერი კარბოქსილის მჟავები ნახშირბადის ატომების რაოდენობა 3-დან 18-მდე. ეს მჟავები ძირითადად შედგება ნახშირბადის ატომების ლუწი რაოდენობისგან. მჟავები სამი და ხუთი ნახშირბადით. ცხიმები და ზეთები გლიცერიდების კომპლექსური ნაზავია, მაგალითად, კარაქს უწოდებენ გლიცერიდს 14 კარბოქსილის მჟავისგან (ცხიმების და ზეთების შემადგენლობა - ცხრილი 1.3.4). გლიცერიდები, რომლებიც მყარია ოთახის ტემპერატურაზე, კლასიფიცირდება როგორც ცხიმები, ხოლო თხევადი გლიცერიდები კლასიფიცირდება როგორც ზეთები.
ცხიმები დიდი ხანია გამოიყენება, როგორც საწყისი პროდუქტი კარბოქსილის მჟავებისა და ტუტე ლითონების მარილების (საპნების) წარმოებაში.ისინი მიიღება ცხიმების ტუტე ჰიდროლიზით. ვინაიდან პროცესი იწვევს საპნებს, მას საპონიფიკაცია ეწოდება.
 1.3.5. კარბოქსილის მჟავების ამიდები.
1.3.5. კარბოქსილის მჟავების ამიდები.
ნაერთებს, რომლებშიც კარბოქსილის ჯგუფის ჰიდროქსილი ჩანაცვლებულია ამიაკის ნარჩენით - ამინო ჯგუფით - ან შემცვლელი ამინო ჯგუფით, ამიდები ეწოდება.
ამიდები უნდა ყოფილიყო მიღებული კარბოქსილის მჟავას ამიაკის რეაქციით. თუმცა ამ რეაქციის შედეგად მიიღება არა ამიდი, არამედ მჟავას ამონიუმის მარილი
ამიდების მომზადება მიიღწევა მარილის გაცხელებით და წყლის ამოღებით დისტილაციით.
გართულებების გარეშე, ჰალოაცილების რეაქცია ამიაკთან და მის წარმოებულებთან სწრაფად და მაღალი მოსავლიანობით მიმდინარეობს.
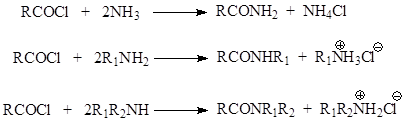
მჟავა ანჰიდრიდები და ეთერები წარმატებით გამოიყენება ამიდების სინთეზისთვის.
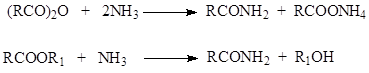
კარბოქსილის მჟავას სხვა წარმოებულების მსგავსად, ამიდები ჰიდროლიზდება როგორც მჟავების, ასევე ფუძეების კატალიზური მოქმედების ქვეშ.

და ეს რეაქცია მიმდინარეობს როგორც ნუკლეოფილური ჩანაცვლება "დამატებით". მინერალური მჟავები ახდენენ მას კატალიზებას კარბონილის ჟანგბადის პროტონაციით და ნახშირბადზე დადებითი მუხტის შექმნით. ეს ხელს უწყობს ნუკლეოფილურ შეტევას ნახშირბადზე

კარბოქსილის მჟავების ამიდების ჰიდროლიზის საბაზო კატალიზი მიმდინარეობს შემდეგი სქემის მიხედვით
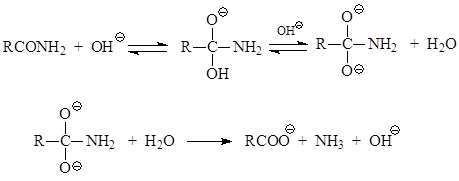
მნიშვნელოვანი ადგილი უჭირავს მათ მიხედვით დაყოფას ჰოფმანი, რომელიც წარმოიქმნება ჰიპოქლორიტების ან ჰიპობრომიტების მოქმედებით. ამ შემთხვევაში პირველადი ამინები მიიღება ნახშირბადის ატომების რაოდენობით 1 ნახშირბადზე ნაკლები, ვიდრე თავდაპირველ ამიდში.
კარბოქსილის მჟავების ამიდები, როდესაც თბება წყლის გამწმენდი საშუალებებით, მაგალითად, ფოსფორის პენტოქსიდით, კარგავს წყლის მოლეკულას და გადაიქცევა მჟავა ნიტრილებად.
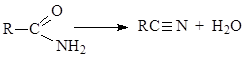
1.3.6. კარბოქსილის მჟავების ნიტრილები.
ნიტრილები ალბათ კარბოქსილის მჟავების ერთადერთი წარმოებულებია, რომლებიც არ შეიცავს კარბონილის ჯგუფს მათ მოლეკულაში.
ნიტრილების მიღება - ალკილის ჰალოიდების რეაქცია ციანიდის იონთან, წყალბადის ციანიდის დამატება ალკინებში და კარბონილის ნაერთებში, ახლახან განხილული კარბოქსილის მჟავას ამიდების გაუწყლოება.
კარბოქსილის მჟავების მიღების მეთოდად დიდი მნიშვნელობა აქვს ნიტრილების ჰიდროლიზს. ეს რეაქცია ხდება როგორც ტუტე, ასევე მჟავე გარემო

მჟავე გარემოში ნიტრილები ჰიდროლიზდება ორ ეტაპად: ჯერ ამიდები და შემდეგ ამიდები კარბოქსილის მჟავებამდე.
ამიდების ჰიდროლიზი განხილული იყო განყოფილებაში 1.3.5.
ნიტრილების სხვა რეაქციებს შორის საინტერესოა ჰიდროგენიზაცია ამინებში, რეაქციები, რომლებიც მოიცავს α-წყალბადის ატომებს, მაგალითად, ალკილაციას.
დ ეკარბოქსილაცია - გაყოფაკარბოქსილის მჟავას მოლეკულიდან ნახშირორჟანგიდა ნახშირწყალბადის წარმოქმნა, რომელიც შეიცავს თავდაპირველ მჟავაზე ერთი ნახშირბადით ნაკლებს
ელექტროლიზიკარბოქსილის მჟავების მარილები კოლბის მიხედვით- ნახშირწყალბადის წარმოქმნა ნახშირბადის ატომების დიდი რაოდენობით
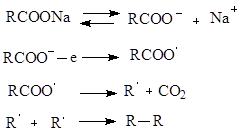
დეკარბოქსილირების რეაქციები ასევე მოიცავს კალციუმის ან კარბოქსილის მჟავების ბარიუმის მარილების პიროლიზს. პირიაკარბონილის ნაერთების წარმოქმნით.
1.3.8. კარბოქსილის მჟავების ჰალოგენაცია α-პოზიციაში.
რეაქცია გელ-ვოლგარდ-ზელინსკიხდება მაშინ, როდესაც მჟავები ჰალოგენდება მცირე რაოდენობით ფოსფორის თანდასწრებით
სხვა α-წყალბადის ატომები ასევე შეიძლება შეიცვალოს ჰალოგენით, ასეთის არსებობის შემთხვევაში. ამის მაგალითია ტრიქლოროძმარმჟავას წარმოება.
გელ-ვოლჰარდ-ზელინსკის რეაქცია მიმდინარეობს ჰალოგენირებული მჟავების მაღალი გამოსავლით. α-ჰალოგენირებული მჟავების მეშვეობით შესაძლებელია კარბოქსილის მჟავების მრავალი წარმოებულის მიღება: ჰიდროქსი- და ამინომჟავები, უჯერი მჟავები და ა.შ.
ლექცია #11
2. უჯერი კარბოქსილის მჟავები.
უჯერი კარბოქსილის მჟავები შეიცავს ორმაგ ან სამმაგ ბმებს და კარბოქსილის ჯგუფებს მათ მოლეკულაში. აქ არის ყველაზე გავრცელებული უჯერი მჟავები და მათი სახელები
CH 2 \u003d CHCOOH აკრილის მჟავა, პროპენოინის მჟავა
CH 3 CH \u003d CHCOOH კროტონული მჟავა, 2-ბუტენოინის მჟავა
ცის-CH 3 (CH 2) 7 CH \u003d CH (CH 2) 7 COOH ოლეინის მჟავა
ტრანსი-CH 3 (CH 2) 7 CH \u003d CH (CH 2) 7 COOH ელაიდური მჟავა
CH 3 (CH 2) 4 CH \u003d CHCH 2 CH \u003d CH (CH 2) 7 COOH ლინოლის მჟავა
CH 3 CH 2 CH \u003d CHCH 2 CH \u003d CHCH 2 CH \u003d CH (CH 2) 7 COOH ლინოლენის მჟავა
ცის-HOOSCH=CHCOOH მალეინის მჟავა, ცის-ბუტენედიოინის მჟავა
ტრანსი-HOOSCH=CHCOOH ფუმარინის მჟავა, ტრანს-ბუტენედიოინის მჟავა
უჯერი კარბოქსილის მჟავები, რომლებშიც ორმაგი ბმა და კარბოქსილის ჯგუფი ამოღებულია ერთმანეთისგან, ავლენენ ჩვეულებრივ თვისებებს, რომლებიც თან ახლავს ალკენებსა და კარბოქსილის მჟავებს. ამიტომ, ამ განყოფილებაში განიხილება მხოლოდ ისეთი უჯერი კარბოქსილის მჟავები, რომლებშიც ფუნქციური ჯგუფები კონიუგირებულია და გავლენას ახდენს ერთმანეთზე.
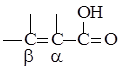
უჯერი კარბოქსილის მჟავების ყველაზე მნიშვნელოვანი წარმომადგენელია აკრილისმჟავა. შემოთავაზებულია ამ მჟავის სინთეზის მრავალი მეთოდი. ერთ-ერთი მათგანის მიხედვით ეთილენქლოროჰიდრინის ან ეთილენის ოქსიდისგანმიიღება ჰიდროქსიპროპიონის მჟავა ნიტრილი, რომელიც მჟავას ჰიდროლიზის შემდეგ, რასაც მოჰყვება გაუწყლოება, გადაიქცევა აკრილის მჟავად.
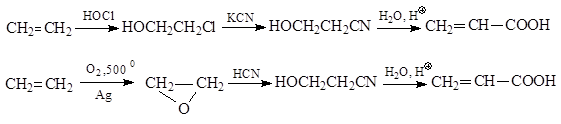
დაფუძნებულია აკრილის მჟავის სინთეზის სხვა მეთოდები აცეტილენის გარდაქმნაზე.ამ შემთხვევაში ან აკრილონიტრილი მიიღება ჰიდროციანმჟავას დამატებით და ჰიდროლიზდება, ან გამოიყენება ოქსიოსინთეზის რეაქცია.
მეთაკრილის მჟავის მიღების ჩვეულებრივი გზაა აცეტონში ჰიდროციანმჟავას დამატება, რასაც მოჰყვება მიღებული ციანოჰიდრინის ჰიდროლიზი და გაუწყლოება.
უჯერი მჟავების კიდევ ერთი წარმომადგენელი - კროტონის მჟავა - შეიძლება მივიღოთ დაჟანგვით კროტონალდეჰიდი, რომელიც არის პროდუქტი აცეტალდეჰიდის კროტონული კონდენსაცია. ამ მჟავის მიღება ასევე შესაძლებელია Knoevenagel რეაქციებიაცეტალდეჰიდის კონდენსაცია მალონის მჟავასთან პირიდინის თანდასწრებით, რასაც მოჰყვება ჩანაცვლებული მალონის მჟავას დეკარბოქსილაცია
ნაერთების დამახასიათებელი თვისება, რომელიც შეიცავს ორმაგი ნახშირბად-ნახშირბადის ბმას, არის შეღწევის უნარი დამატების რეაქციაში. სადაც ვლინდება სუსტი π-ბმა დამის ნაცვლად არსებობს ორი ძლიერი σ-ბმაუჯერი კარბოქსილის მჟავები შედის ელექტროფილურ დამატებით რეაქციებში, მაგრამ უარესი ვიდრე ალკენები. ისინი ასევე შედიან ნუკლეოფილურ დამატებით რეაქციებში.
ელექტროფილური დამატება. განვიხილოთ აკრილის მჟავის რეაქცია წყალბადის ქლორიდთან. Თუ პირველი ეტაპიეს რეაქცია - პროტონაცია - წარმოვიდგინოთ უბრალოდ როგორც პროტონის დამატება ორმაგ ბმა ნახშირბადში, მაშინ ამის შედეგად შესაძლებელია I და II იონების წარმოქმნა. ამ იონების სტაბილურობაზე მსჯელობა საკმაოდ რთულია. თუ - I პირველადია, მაშინ II, თუმცა მეორადი, დესტაბილიზებულია მეზობელი კარბოქსილის ჯგუფის მიერ
აკრილის მჟავა არის ორმაგი ბმების კონიუგირებული სისტემა, როგორც ბუტადიენის მოლეკულაში. მისი სტრუქტურის მიხედვით, აკრილის მჟავას შეუძლია პროტონატი ტერმინალურ ატომებზეკონიუგირებული სისტემა კვლავ II-ის ფორმირებით და რეზონანსულად სტაბილიზირებული კარბოკაციით, რომელიც წარმოდგენილია III და IV სტრუქტურებით
ქლორის ანიონის IV-ში შემდგომი დამატება მისცემს რეაქციის პროდუქტის ენოლის ფორმას, რომელიც შედის ტავტომერულ ურთიერთობაში მის კეტო ფორმასთან.
თანამედროვე ცნებების მიხედვით, მარკოვნიკოვის წესი განმარტებულია, როგორც იონური დამატება C=C - ბმა, რომელიც მიმდინარეობს უფრო სტაბილური კარბოკატიონის წარმოქმნით. ეს არის ზუსტად ის, რაც ხდება α, β-უჯერი კარბოქსილის მჟავების ელექტროფილური დამატების დროს. ასევე ხდება განხილული ტიპის სხვა რეაქციები, მაგალითად, დატენიანება
Ამგვარად, კარბოქსილის ჯგუფი ორმაგ ბმაზე არა მხოლოდ ამცირებს მის რეაქტიულობას ელექტროფილურ რეაგენტებთან მიმართებაში, არამედ გავლენას ახდენს მიმაგრების მიმართულებაზე.
ნუკლეოფილური დანამატი. კარბოქსილის ჯგუფის გამააქტიურებელი ეფექტის გამო, α, β - უჯერი კარბოქსილის მჟავები ძალიან მზად არიან შევიდნენ ნუკლეოფილურ დამატების რეაქციებში. მაგალითები შეიძლება იყოს აკრილის მჟავას დამატება ამიაკი ჰიდროქსილამინი და ჰიდროციანმჟავა

უჯერი კარბოქსილის მჟავებზე ნუკლეოფილური დამატების შემოთავაზებული მექანიზმი შემდეგია
ნუკლეოფილური რეაგენტი მიმაგრებულია კონიუგირებული სისტემის ტერმინალურ ატომზერეზონანსულად სტაბილიზირებული კარბანიონის წარმოქმნით, რომელიც შემდგომ რეაქციის საფეხურზე ამოიღებს პროტონსგამხსნელის მოლეკულიდან და გადაიქცევა პროდუქტად.
უჯერი კარბოქსილის მჟავებზე ნუკლეოფილური დანამატის რეაქციებს შორის არის ასევე მაიკლის რეაქცია, რომელიც არის კარბანიონის დამატება α, β - უჯერი ნაერთებში. Როგორც მაგალითი ვაძლევთ ეთილის კროტონატის რეაქციას ეთილის მეთილის მალონატთანდა რეაქცია ეთილის მეთაკრილატი ეთილის ციანოაცეტატითნატრიუმის ეთოქსიდის თანდასწრებით
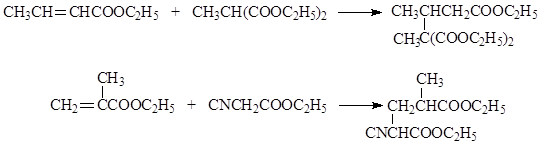
მაიკლის რეაქციის განსაკუთრებული შემთხვევაა აკრილონიტრილის, როგორც უჯერი კომპონენტის გამოყენება, რომელსაც ტუტე გარემოში შეუძლია წყალბადის მოძრავი ატომით რამდენიმე ნაერთების მიმაგრება. ეს საშუალებას გაძლევთ გააფართოვოთ სინთეზური ორგანული ქიმიის შესაძლებლობები. აქ მოცემულია აკრილონიტრილთან რეაქციების რამდენიმე მაგალითი
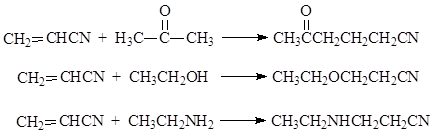
ყველა ამ რეაქციაში დანამატი მიდის აკრილონიტრილის β - ნახშირბადის ატომში და მოლეკულაში. აქტიური წყალბადის ნაცვლად შემოტანილია ატომების დაჯგუფება -CH 2 CH 2 CN.ამის საფუძველზე განხილულ რეაქციას ხშირად უწოდებენ ციანოეთილის რეაქცია.
განსაკუთრებული მნიშვნელობა უჯერი კარბოქსილის მჟავებიდა მათი წარმოებულები დევს მათში ძვირფას პროდუქტებად პოლიმერიზაციის უნარი.
პოლიმერიზაციის დროს აკრილონიტრილი იძლევა პოლიმერს, საიდანაც მზადდება ქიმიური ბოჭკოები - მატყლის შემცვლელი. როდესაც აკრილონიტრილის კოპოლიმერიზაცია ხდება ბუტადიენთან, მიიღება ზეთი და ბენზინისადმი მდგრადი სინთეზური რეზინები.
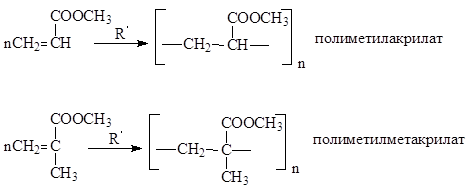
ასევე ფართოდ ცნობილია აკრილის და მეტაკრილის მჟავების მეთილის ეთერების პოლიმერები,წარმოადგენს არის უფერო, გამჭვირვალე მასალები, რომელთა ჩამოსხმაც შესაძლებელია. მათ ასევე უწოდებენ ორგანულ სათვალეებს.
ლექცია #12
3. დიკარბოქსილის მჟავები.
შემზღუდველი დიკარბოქსილის მჟავები შეიცავს ორ კარბოქსილის ჯგუფს მათ მოლეკულაში. ისინი თავიანთ სახელს ყველაზე ხშირად ტრივიალური ნომენკლატურიდან იღებენ. სისტემური ნომენკლატურის მიხედვით, მჟავაში ორი კარბოქსილის არსებობა ნაჩვენებია დაბოლოების დამატებით. დიური მჟავანახშირწყალბადის სახელს, რომელიც ამ ნაერთში შეესაბამება ნახშირბადის ატომების ყველაზე გრძელ ჯაჭვს. ქვემოთ მოცემულია ყველაზე გავრცელებული დიკარბოქსილის მჟავები და მათი სახელები.
HOOC-COOH ოქსილის მჟავა, ეთანი დიოვაიამჟავა
HOOS-CH 2 -COOH მალონის მჟავა, პროპანი დიოვაიამჟავა
HOOS-(CH 2) 2 -COOH სუქცინის მჟავა, ბუტანი დიოვაიამჟავა
HOOS-(CH 2) 3 -COOH გლუტარის მჟავა, პენტანი დიოვაიამჟავა
HOOS-(CH 2) 4 -COOH ადიპინის მჟავა, ჰექსანდიოინის მჟავა
HOOS-(CH 2) 5 -COOH პიმელის მჟავა, ჰეპტანედიოინის მჟავა
HOOS-(CH 2) 6 -COOH სუბერინის მჟავა, ოქტანდიოინის მჟავა
HOOS-(CH 2) 7 -COOH აზელაინის მჟავა, არაანდიოინის მჟავა
HOOC-(CH 2) 8 -COOH სებაციუმის მჟავა, დეკანდიოინის მჟავა
ორფუძიანი მჟავების მისაღებად გამოიყენება იგივე მეთოდები, რაც მონობაზური მჟავების სინთეზისთვის: პირველადი სპირტების და ალდეჰიდების დაჟანგვა, ნიტრილების და მჟავა წარმოებულების ჰიდროლიზი და ა.შ. იმისათვის, რომ არ გავიმეოროთ, მათ არ განვიხილავთ. ბევრად უფრო საინტერესო აპლიკაცია საერთო მეთოდებისპეციფიკური მჟავების სინთეზამდე, აგრეთვე მიღების სპეციალური მეთოდების გამოყენებამდე.
ოქსილის მჟავა. მარილების სახით გვხვდება მრავალ მცენარეში (მჟავე, ოქსილისში). ინჟინერიაში მიიღება ჭიანჭველა მჟავას 400 0 ნატრიუმის ან კალიუმის მარილზე გაცხელებით
საინტერესოა აღინიშნოს, რომ შემოთავაზებული იყო ოქსილის მჟავის პირველი სინთეზი ციანოგენის ჰიდროლიზით. ვეჰლერიჯერ კიდევ 1824 წელს
მალონის მჟავა. ამ მჟავის სინთეზის ჩვეულებრივი გზა, რომელიც განსაკუთრებულ როლს ასრულებს ორგანული სინთეზი, შედგება მისი მონონიტრილის ჰიდროლიზში
შეიძლება გამოყენებულ იქნას სხვა მეთოდები, მაგალითად, მეთილენქლორიდის დინიტრილში გადაქცევა და მისი ჰიდროლიზი, ორგანომაგნიუმის სინთეზის გამოყენება.
სუქცინის მჟავაჩვეულებრივ მიიღება მალეინის ანჰიდრიდის ჰიდროგენაციით, ბენზოლის დაჟანგვის პროდუქტი. როგორც მალონის მჟავას სინთეზში, ასევე შეიძლება გამოყენებულ იქნას დინიტრილის ჰიდროლიზი. თავად დინიტრილი მიიღება 1,2-დიქლორეთანის ნუკლეოფილური ჩანაცვლებით.
ადიპინის მჟავატექნოლოგიაში in დიდი რაოდენობითთურმე ციკლოჰექსანის დაჟანგვა აზოტის მჟავითერთ ეტაპზე ან შუალედური დაჟანგვის პროდუქტების - ციკლოჰექსანოლისა და ციკლოჰექსანონის მეშვეობით, რომლებიც კიდევ უფრო ადვილად იჟანგება
თავისით ქიმიური თვისებებიორფუძიანი მჟავები ახლოსაა მონობაზის მჟავებთან. ისინი ქმნიან ყველა ცნობილ მჟავას წარმოებულს ერთი (მჟავის წარმოებულები) ან ორივე კარბოქსილის ჯგუფის მონაწილეობით (სრული წარმოებულები). ამასთან, ორი კარბოქსილის ურთიერთგავლენა, განსაკუთრებით მაშინ, როდესაც ისინი ერთმანეთთან ახლოს არიან განლაგებული, იწვევს მათ ქცევაში სპეციფიკური მახასიათებლების გამოჩენას ქიმიურ რეაქციებში. განვიხილოთ ეს მახასიათებლები.
3.1. მჟავიანობა. ცხადია, რომ ორფუძიან მჟავებს აქვთ მჟავიანობის ორი მუდმივი, რომლებიც დაკავშირებულია ერთი ან მეორე კარბოქსილის ჯგუფის დისოციაციასთან.
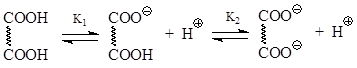
როდესაც ერთ-ერთი კარბოქსილი იშლება, მეორე უბრალოდ მოქმედებს როგორც ელექტრონის ამომყვანი ჯგუფი. მონოკარბოქსილის მჟავების მჟავიანობის განხილვისას (ნაწილი 1.3.1), აღმოჩნდა, რომ ასეთი შემცვლელები აძლიერებენ მჟავე თვისებებს. ამ მიზეზით, მჟავიანობის პირველი მუდმივი (K 1) ორფუძიანი მჟავებისთვის გაცილებით მაღალია, ვიდრე მონობაზური მჟავებისთვის. ამავდროულად, მჟავიანობის მეორე მუდმივი (K 2 ) მნიშვნელოვნად დაბალია, რადგან მეორე კარბოქსილის იონიზაციის დროს პროტონი უნდა მოიხსნას ორმაგად დამუხტული ანიონიდან. ქვემოთ მოცემული მონაცემები საშუალებას გვაძლევს რაოდენობრივ დონეზე განვიხილოთ ორფუძიანი მჟავების მჟავიანობა.
მჟავა 10 5 კ 1 10 5 კ 2
ფორმაკი 17.7 -
ძმარი 1.75 -
მჟავე 5400 5.2
მალონიკი 140 0.20
ქარვა 6.4 0.23
გლუტარიკი 4,5 0,38
ადიპიკი 3.7 0.39
3.2. პ ოლიკონდენსაცია. ჩვეულებრივი ქიმიური რეაქციები მათში ორფუძიანი მჟავების მონაწილეობის შემთხვევაში შეიძლება იწვევს პოლიმერული მოლეკულების წარმოებას . მართალია, რომ ეს მოხდეს, მჟავას ქიმიური რეაქციის პარტნიორიც უნდა იყოს ორფუნქციური. მაგალითად, ძმარმჟავას რეაქცია ეთილამინთან უბრალოდ მისცემს ეთილაცეტამიდს.
Იმ შემთხვევაში, თუ ორფუძიანი მჟავა და დიამინი, შესაძლებელი ხდებამრავალი მჟავისა და ამინის მოლეკულის რეაქცია პოლიმერული პოლიამიდის წარმოქმნა. ადიპინის მჟავისა და ჰექსამეთილენდიამინის რეაქციაში მონაწილეობით წარმოიქმნება პოლიამიდი ( ნეილონი), რომელიც მოიცავს მჟავას და ამინის ნარჩენებს, რომლებიც დაკავშირებულია ე.წ
პოლიმერიზაციისგან განსხვავებით, ჩვეულებრივი ქიმიური რეაქციების საფუძველზე პოლიმერების წარმოებას ე.წ პოლიკონდენსაცია. პოლიკონდენსაციას ყოველთვის ახლავს უფრო მარტივი მოლეკულების გამოყოფა წყლის განხილულ შემთხვევაში.
3.3. დამოკიდებულება გათბობამდე. დიკარბოქსილის მჟავების გაცხელების შედეგი განისაზღვრება მათი სტრუქტურით. ზოგადად, სითბოს გავლენით მჟავის მოლეკულა იშლება. ამ შემთხვევაში გამოიყოფა მოლეკულები ან ნახშირორჟანგი და წარმოიქმნება მონობაზური მჟავები, ციკლური ანჰიდრიდები და ციკლური კეტონები.
გლუტარის და სუქცინის მჟავები გაცხელებისას განიცდიან ინტრამოლეკულურ დეჰიდრატაციას ციკლური ანჰიდრიდების წარმოქმნით.
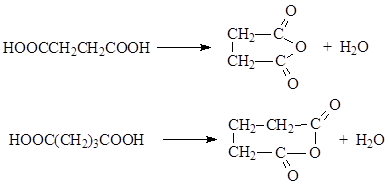
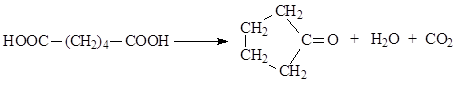
4. ოქსომჟავები.
ოქსომჟავები შეიცავს კარბოქსილის და კარბონილის ჯგუფებს მათ მოლეკულაში. კარბონილის ჯგუფი შეიძლება წარმოდგენილი იყოს ალდეჰიდის ან კეტო ჯგუფებით . გარკვეული ფუნქციური ჯგუფების შემცველობისა და მოლეკულაში მათი შედარებითი პოზიციის მიხედვით, ზოგიერთი ოქსომჟავა განსხვავდება სხვებისგან. აქ არის რამოდენიმე ყველაზე გავრცელებული ოქსომჟავა და მათი სახელები.
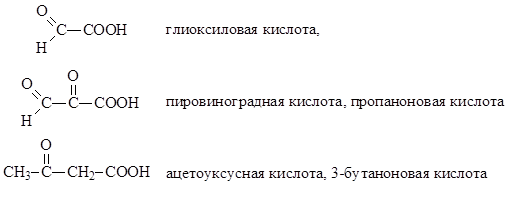 ოქსომჟავები ორფუნქციური ნაერთებია. მათი სინთეზის მეთოდების განხილვისას სავსებით გონივრულია დავეყრდნოთ უკვე ცნობილ ინფორმაციას კარბონილისა და კარბოქსილის ჯგუფების შექმნის შესახებ. იგივე შეიძლება ითქვას ოქსომჟავების თვისებებზე. ეს საშუალებას გვაძლევს განვიხილოთ ოქსომჟავები მხოლოდ ერთი მათგანის მაგალითის გამოყენებით, თუმცა ყველაზე ცნობილი არის აცეტოძმარმჟავა და მისი ეთილის ეთერი.
ოქსომჟავები ორფუნქციური ნაერთებია. მათი სინთეზის მეთოდების განხილვისას სავსებით გონივრულია დავეყრდნოთ უკვე ცნობილ ინფორმაციას კარბონილისა და კარბოქსილის ჯგუფების შექმნის შესახებ. იგივე შეიძლება ითქვას ოქსომჟავების თვისებებზე. ეს საშუალებას გვაძლევს განვიხილოთ ოქსომჟავები მხოლოდ ერთი მათგანის მაგალითის გამოყენებით, თუმცა ყველაზე ცნობილი არის აცეტოძმარმჟავა და მისი ეთილის ეთერი.
აცეტოძმარმჟავა მიეკუთვნება β-ოქსო მჟავებს. ამ მჟავის მიღების ძირითადი მეთოდია ეთერების კონდენსაცია ალკოჰოლატების თანდასწრებით. ეს რეაქცია, რომელსაც ეწოდება კლაიზენის რეაქცია, უკვე განხილულია აცეტოძმარმჟავას ეთერის სახით მიღების განყოფილებაში, რეაქცია შორის დიკეტენი და ეთილის სპირტი
მისი ქიმიური თვისებების მიხედვით, აცეტოძმარმჟავა წააგავს კეტონებსა და მჟავებს. კარბოქსილის ჯგუფის მიხედვით იძლევა მჟავებისთვის საერთო წარმოებულებს: მარილებს, ამიდებს, ეთერებს და ა.შ.
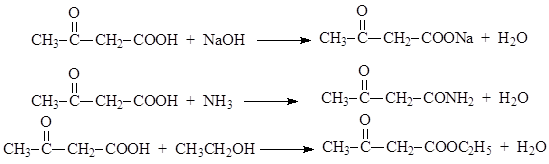
უფრო სტაბილურია, ვიდრე თავად მჟავა, აცეტოძმარმჟავას ეთერი კარბონილის ჯგუფში ამატებს ჰიდროციანმჟავას, ნატრიუმის ბისულფიტს, წყალბადს იზოლაციის დროს, ფენილჰიდრაზინს და ა.შ.

აცეტოაცეტატური ესტერი და არის უჯერი ალკოჰოლი, რომელიც წონასწორობაშია თავის კეტო ფორმასთან

ყველა ზემოხსენებულ რეაქციაში აცეტოაცეტატური ესტერი შედის ენოლის სახით

აცეტოაცეტატური ეთერის კეტო-ენოლის ნარევის შემადგენლობა ცნობილი გახდა გერმანელი მკვლევარის მუშაობის წყალობით. ნორ(1911 წ.).
აცეტოაცეტური ეთერის -78 0-მდე გაციებისას ეთერ-ჰექსანის ნარევში, კნორმა გამოყო მყარი მ.პ. -39 0 . ეს ნივთიერება არ აფერხებდა ბრომიან წყალს და არ რეაგირებდა რკინის ქლორიდთან. ამ მონაცემებიდან გამომდინარეობდა, რომ ნივთიერება ასე pl. -39 0 არის ეთერის კეტო ფორმა.
აცეტოაცეტური ეთერის მეტალის ნატრიუმთან რეაქციით, ნორმა მიიღო ნატრაცეტოაცეტატური ესტერი. მშრალი HCl გადადიოდა ამ ნივთიერების სუსპენზიის მეშვეობით ნავთობის ეთერში. ამან გამოყო ზეთი, რომელიც მყისიერად რეაგირებდა ბრომთან და რკინის ქლორიდთან. ეს იყო აცეტოაცეტატური ეთერის ენოლის ფორმა. ამრიგად, ნორმა პირველმა შეძლო ტავტომერების გამოყოფა
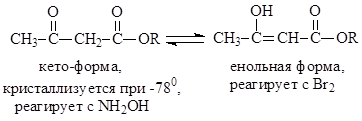
უფრო მეტიც, აღმოჩნდა, რომ ტავტომერების შენახვა შესაძლებელია დიდი ხნის განმავლობაში -78 0-ზე.
აცეტოძმარმჟავაზე დაფუძნებული სინთეზები. საკმაოდ ადვილად დეკარბოქსილირდება გაცხელებისას. ეს წარმოქმნის კეტონს.
აცეტოაცეტური მჟავა გამოიყენება ორგანულ სინთეზში მონო- და ორგანზომილებიან აცეტონების მისაღებად.
5. ჰიდროქსი მჟავები.
ჰიდროქსი მჟავები შეიცავს ჰიდროქსილის და კარბოქსილის ჯგუფებს მათ მოლეკულაში. ჰიდროქსილებისა და კარბოქსილების რაოდენობა ჰიდროქსი მჟავებში განსაზღვრავს მათ ატომურობას და ფუძეულობას. გარდა ამისა, ჰიდროქსი მჟავები ასევე განსხვავდებიან მოლეკულაში ფუნქციური ჯგუფების შედარებითი განლაგებით. ყველაზე გავრცელებული ჰიდროქსი მჟავები და მათი სახელები მოცემულია ქვემოთ (მჟავას სტერეოქიმიის გამოკლებით)
5.1. მიღების მეთოდები. როგორც ოქსომჟავების შემთხვევაში, ჰიდროქსი მჟავები მიიღება შესაბამისი ფუნქციური ჯგუფების - ჰიდროქსილისა და კარბოქსილის შექმნის უკვე ცნობილი მეთოდების გამოყენებით.
α - ჰიდროქსი მჟავები ჩვეულებრივ სინთეზირდება შესაბამისი ციანოჰიდრინის ჰიდროლიზით ან α - ჰალოგენირებული მჟავების ჰიდროლიზით.

β - ჰიდროქსი მჟავების მისაღებად, შეგიძლიათ გამოიყენოთ მსგავსი მეთოდები. თუმცა, არსებობს ამისთვის კონკრეტული მეთოდი - რეფორმატსკის რეაქცია.ეს რეაქცია მოიცავს ალდეჰიდების და კეტონების ურთიერთქმედებას α-ბრომოესტერებთან და მეტალის თუთიასთან ეთერის ხსნარში. ამ შემთხვევაში ჰიდროქსიმჟავას ესტერი მიიღება ალკოჰოლატის სახით, რომლის ჰიდროლიზი უკვე იწვევს თავად ჰიდროქსი მჟავას.
დადგენილია, რომ თავდაპირველად ბრომოესტერი თუთიასთან ურთიერთქმედებს და წარმოქმნის თუთიის ორგანულ ნაერთს, რომელიც შემდგომ ემატება ალდეჰიდის ან კეტონის კარბონილის ჯგუფს.

ეს ყველაფერი ანალოგიურია გრიგნარდის რეაგენტის მომზადებისა და რეაქციისა. რეფორმატსკის რეაქციის მახასიათებელია თუთიის გამოყენება მაგნიუმის ნაცვლად და მხოლოდ α - ბრომოესტერები. აღმოჩნდა, რომ თუთიის ორგანული ნაერთები, ორგანომაგნიუმის ნაერთებისგან განსხვავებით, ნაკლებად რეაქტიულია. მათ შეუძლიათ რეაგირება მხოლოდ ალდეჰიდებისა და კეტონების კარბონილებთან, ეთერულ ჯგუფზე გავლენის გარეშე.
5.2. ქიმიური თვისებები. ჰიდროქსი მჟავებს ავლენენ ალკოჰოლებისა და მჟავების თანდაყოლილი თვისებები. კარბოქსილის ჯგუფის მიხედვით, ისინი იძლევიან კარბოქსილის მჟავების ყველა წარმოებულს
სპირტების მსგავსად რეაგირებენ, ისინი აძლევენ ალკოჰოლატებს, ეთერებს, ანაცვლებენ ჰიდროქსილს ჰალოგენით
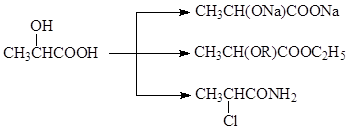
ზოგჯერ ფუნქციონალურ ჯგუფებს შორის კონკურენციაა. ასეთ შემთხვევებში რეაქციის რეგიოშერჩევითობა განისაზღვრება რეაგენტისა და რეაქციის პირობების არჩევით. ამგვარად, ჰალოგენზე წყალბადის ჰალოგენების მოქმედებით, მხოლოდ ალკოჰოლის ჰიდროქსილი იცვლება. ფოსფორის პენტაქლორიდის გამოყენების შემთხვევაში - როგორც სპირტი, ასევე კარბოქსილის ჰიდროქსილები.
ჰიდროქსი მჟავების შემთხვევაში რეაქციის რეაქტიულობასა და მიმართულებაზე ფუნქციური ჯგუფების ურთიერთგავლენის პრობლემის განხილვა დიდ ინტერესს იწვევს.
α - ჰიდროქსი მჟავები ადვილად იშლება კარბოქსილის მჟავებამდე
მჟავებით გაცხელებისას α-ჰიდროქსი მჟავები ადვილად იშლება ჭიანჭველა მჟავას
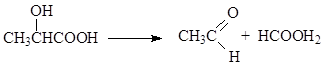
ჰიდროქსი მჟავების დეჰიდრატაციის შედეგი დამოკიდებულია ჰიდროქსილის და კარბოქსილის ჯგუფების შედარებით პოზიციაზე.
β - ჰიდროქსიკარბოქსილის მჟავები ისე შლის წყალს, რომ რეაქციის შედეგად მიიღება α, β - უჯერი კარბოქსილის მჟავები, რომელშიც C=C- და C=O- კავშირები კონიუგირებულია
α - ჰიდროქსი მჟავები, გაცხელებისას, იშლება წყალი ორი მოლეკულის ურთიერთესტერიფიკაციის შედეგად ციკლური ეთერების წარმოქმნით, ე.წ. ლაქტიდები
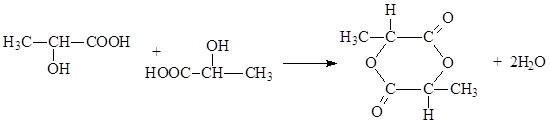
ბოლოს აღვნიშნავთ, რომ γ - და δ - ჰიდროქსი მჟავები გაცხელებისას განიცდიან ინტრამოლეკულურ ესტერიფიკაციას. ამ შემთხვევაში წარმოიქმნება ხუთ და ექვსწევრიანი ციკლური ეთერები, რომლებსაც γ- და δ-ლაქტონები უწოდებენ.

ჰიდროქსი მჟავებმა (ტარტარულმა მჟავებმა) გამორჩეული როლი ითამაშეს ენატიომერიზმის ფენომენის აღმოჩენასა და ამ ტიპის სივრცითი იზომერიზმის კანონზომიერებების შესწავლაში.
1848 წელს ლუი პასტერმა, ღვინის მჟავების შესწავლისას, აღმოაჩინა, რომ ერთ-ერთი მათგანის ნატრიუმის ამონიუმის ტარტრატი (ტარტრატები - ღვინის მჟავას მარილები), განზავებული წყალხსნარებიდან კრისტალიზებისას წარმოქმნის კრისტალების ორ ტიპს. ყურძნის წვენისგან გამოყოფილი მჟავის ეს კრისტალები, რომელსაც უწოდებენ ყურძნის ან რასემულ (ლათ. racemus - ყურძნის) მჟავას, ძალიან ოდნავ განსხვავდებოდნენ, როგორც საგანი და მისი სარკისებური გამოსახულება. მიუხედავად ამისა, პასტერმა მოახერხა მათი გამოყოფა და აჩვენა, რომ ერთი ტიპის კრისტალები ბრუნავს პოლარიზებული სინათლის სიბრტყეს მარჯვნივ, მეორე ტიპის - მარცხნივ. ამ კვლევებმა შესაძლებელი გახადა იმის დადგენა, რომ იზომერული ტარტარული მჟავები არის დექსტროროტორული და ლევოროტორული. ამ მჟავების თანაბარი რაოდენობით შემდგარ ნარევს რასემიური ეწოდება. ასეთ ნარევს (ტარტარულ მჟავას) არ შეუძლია ბრუნოს პოლარიზებული სინათლის სიბრტყეები იზომერებით ბრუნვის კომპენსაციის გამო. გარდა ამისა, ცნობილია ღვინის მჟავების კიდევ ერთი იზომერი (მეზოტარტარული მჟავა), რომელიც წარმოადგენს შიდა რაცემატს. ამ შემთხვევაში, სინათლის ბრუნვა ზედამოლეკულა ნადგურდება მოლეკულის ქვედა ნაწილის საპირისპირო ნიშნით და ტოლი სიდიდის ბრუნვით.
გრაფიკულად, ღვინის მჟავების იზომერები შეიძლება წარმოდგენილი იყოს შემდეგი პროექციის ფორმულებით:
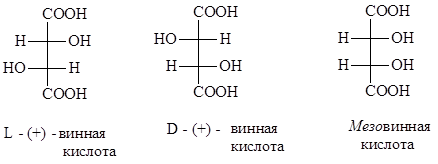
ერთი ორმაგი ბმის მქონე უჯერი მონობაზური მჟავების შემადგენლობა შეიძლება გამოიხატოს ზოგადი ფორმულით C n H 2 n -1 COOH. როგორც ნებისმიერ ორფუნქციურ ნაერთს, მათ ახასიათებთ როგორც მჟავების, ასევე ოლეფინების რეაქციები. α.β-უჯერი მჟავები გარკვეულწილად უფრო ძლიერია, ვიდრე შესაბამისი ცხიმოვანი მჟავები, ვინაიდან კარბოქსილის ჯგუფის გვერდით განლაგებული ორმაგი ბმა აძლიერებს მის მჟავე თვისებებს.
აკრილის მჟავა. უმარტივესი უჯერი მონობაზური მჟავა
ოლეინის, ლინოლეინის და ლინოლენის მჟავები.
ოლეინის მჟავა C 17 H 33 COOH გლიცეროლის ეთერის სახით ძალზე გავრცელებულია ბუნებაში. მისი სტრუქტურა გამოიხატება ფორმულით
ოლეინის მჟავა არის უფერო ცხიმიანი სითხე, უფრო მსუბუქი ვიდრე წყალი, სიცივეში გამკვრივდება ნემსის ფორმის კრისტალებში, დნება 14 ° C ტემპერატურაზე. ჰაერში ის სწრაფად იჟანგება და ყვითლდება.
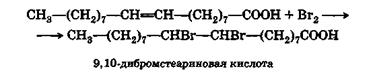 ოლეინის მჟავას მოლეკულას შეუძლია დააკავშიროს ორი ჰალოგენის ატომები:
ოლეინის მჟავას მოლეკულას შეუძლია დააკავშიროს ორი ჰალოგენის ატომები:
კატალიზატორების თანდასწრებით, როგორიცაა Ni, ოლეინის მჟავა ამატებს წყალბადის ორ ატომს, გადაიქცევა სტეარის მჟავად.
ოლეინის მჟავა არის ცის იზომერი (ყველა ბუნებრივი უჯერი მაღალი მოლეკულური წონის მჟავა, როგორც წესი, მიეკუთვნება cis სერიას).
ლინოლის C 17 H 31 COOH და ლინოლენის C 17 H 29 COOH მჟავები კიდევ უფრო უჯერია ვიდრე ოლეინის მჟავა. ეთერების სახით გლიცერინით - გლიცერიდები- ისინი არიან მთავარი შემადგენელი ნაწილიასელის და კანაფის ზეთები:
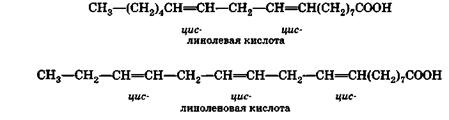
ლინოლეინის მჟავას მოლეკულას აქვს ორი ორმაგი ბმა. მას შეუძლია წყალბადის ან ჰალოგენის ოთხი ატომის მიმაგრება. ლინოლეინის მჟავას მოლეკულას აქვს სამი ორმაგი ბმა, ამიტომ მას უერთდება ექვს წყალბადის ან ჰალოგენის ატომს. ორივე მჟავა წყალბადის დამატებით გადადის სტეარის მჟავაში.
სორბინის მჟავა
მას აქვს ორი ორმაგი ბმა, რომლებიც კონიუგირებულია ერთმანეთთან და კარბოქსილის ჯგუფთან, რომელსაც აქვს ტრანს კონფიგურაცია; ბევრისთვის შესანიშნავი კონსერვანტია საკვები პროდუქტები: ბოსტნეულის კონსერვი, ყველი, მარგარინი, ხილი, თევზი და ხორცპროდუქტები.
მალეინის და ფუმარინის მჟავები. უმარტივესი ორფუძიანი მჟავები, რომლებიც შეიცავს ეთილენურ კავშირს, არის ორი სტრუქტურული იზომერი:
გარდა ამისა, ამ მჟავებიდან მეორესთვის შესაძლებელია ორი სივრცითი კონფიგურაცია:

ფუმარინის მჟავა გვხვდება ბევრ მცენარეში, განსაკუთრებით სოკოში. მალეინის მჟავა ბუნებაში არ არის ნაპოვნი.
ორივე მჟავა ჩვეულებრივ მიიღება ვაშლის (ოქსისაქცინის) მჟავას გაცხელებით:
ნელი, ფრთხილად გაცხელებით ძირითადად მიიღება ფუმარინის მჟავა; ვაშლის მჟავას უფრო ინტენსიური გაცხელებით და დისტილაციით მიიღება მალეინის მჟავა.
ორივე ფუმარიული და მალეინის მჟავები, როდესაც შემცირდება, იძლევა იგივე სუქცინის მჟავას.
ნომენკლატურა.კარბოქსილის მჟავების სერიაში ყველაზე ხშირად გამოიყენება ტრივიალური სახელები, რომელთაგან ბევრი მიუთითებს კარბოქსილის მჟავების წყაროზე.
სისტემატური ნომენკლატურის მიხედვით, კარბოქსილის მჟავების სახელწოდება წარმოიქმნება შესაბამისი ალკანების სახელიდან დაბოლოებით "ოვა" და სიტყვა "მჟავა". ნახშირწყალბადის ჯაჭვის ნუმერაცია იწყება კარბოქსილის ჯგუფის ნახშირბადიდან.
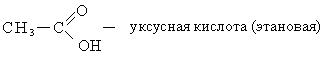


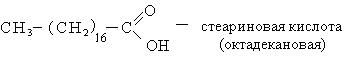
მიღების გზები.ცნობილია მჟავების მომზადების მთელი რიგი ზოგადი მეთოდი.
1. პარაფინური ნახშირწყალბადების კატალიზური დაჟანგვა ატმოსფერული ჟანგბადით:
მრეწველობაში კარბოქსილის მჟავების მისაღებად გამოიყენება პარაფინური ნახშირწყალბადები ნახშირბადის ატომების რაოდენობით C 20 - C 40 და მიიღება C 10 - C 20 მჟავები.
2. ოქსოსინთეზის რეაქცია:
3. ალდეჰიდების დაჟანგვა:

მჟავების სინთეზისთვის აუცილებელი ალდეჰიდები მიიღება კუჩეროვის რეაქციით ან ალკოჰოლების კატალიზური დეჰიდროგენით.
4. ნიტრილების ჰიდროლიზი:
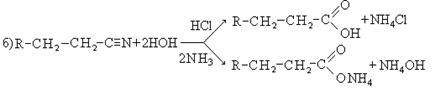
5. გემინალური ჰალოგენის წარმოებულების ჰიდროლიზი:

6. ცხიმების ჰიდროლიზი:

კარბოქსილის მჟავების ქიმიური თვისებები.კარბოქსილის მჟავების ქიმიური თვისებები განისაზღვრება იმ ელექტრონული ეფექტებით, რომლებიც მოქმედებს კარბოქსილის ჯგუფში და მთლიანად მოლეკულაში.
მოლეკულის ელექტრონული სტრუქტურა შესაძლებელს ხდის განასხვავოს კარბოქსილის მჟავების ქიმიური რეაქციების მიმდინარეობის შემდეგი ძირითადი მიმართულებები:
- უწყვეტი რეაქციები O-N კავშირები(I მიმართულება);
- უწყვეტი რეაქციები C-O კავშირები(II მიმართულება);
- რეაქციები ნახშირწყალბადის რადიკალში (III მიმართულება).
I. მჟავების მჟავატუტოვანი თვისებები (I მიმართულება). კარბონილის ჯგუფის ჟანგბადის გავლენა იწვევს ნახშირბადის ატომზე ნაწილობრივ დადებითი მუხტის დაგროვებას, რაც, თავის მხრივ, ინდუქციური ეფექტის გამო, იწვევს ელექტრონის სიმკვრივის მნიშვნელოვან შემცირებას ჰიდროქსილის ჯგუფის ჟანგბადზე. , რის შედეგადაც პროტონი პრაქტიკულად არ ჩერდება, ის ადვილად იშლება და მჟავებს გამოხატული მჟავე თვისებები აქვთ.
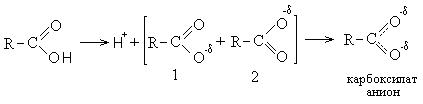
მჟავების დისოციაცია პროტონის განცალკევებასთან ერთად ასევე ენერგიულად ხელსაყრელია, რადგან ამ შემთხვევაში წარმოიქმნება კარბოქსილატური ანიონი, რომელიც სტაბილიზდება რეზონანსით და აქვს უფრო დაბალი ენერგია, ვიდრე ორიგინალური მჟავა. კარბოქსილატის ანიონი არის ორი სტრუქტურის (1 და 2) ჰიბრიდი, რომელიც სტაბილიზირებულია რეზონანსით. კარბოქსილატ ანიონში ატომი sp 2 - ჰიბრიდიზაციის მდგომარეობაშია. ნახშირბადის დაუწყვილებელი p-ელექტრონი თანაბრად გადაფარავს ჟანგბადის ორი ატომის p-ელექტრონს.
ჰალოგენის არსებობა ალკილის რადიკალში აძლიერებს მჟავების მჟავე თვისებებს. ყველაზე ძლიერი მჟავა არის ტრიქლოროძმარმჟავა. პროტონის აბსტრაქციის სიმარტივე ტრიქლოროძმარმჟავაში აიხსნება ჰალოგენის უარყოფითი ინდუქციური ეფექტით, რაც ამცირებს ელექტრონის სიმკვრივეს კარბოქსილატ ანიონზე და ახდენს მის დესტაბილიზაციას.

ჰალოგენირებული კარბოქსილის მჟავების მჟავიანობა იცვლება შემდეგი თანმიმდევრობით:
დონორი შემცვლელების არსებობა ალკილის რადიკალში ზრდის ელექტრონის სიმკვრივეს კარბოქსილატ ანიონზე და პროტონი უფრო ძლიერად ინარჩუნებს მას.
ამ სერიაში ჭიანჭველა უფრო მჟავეა ვიდრე ძმარმჟავა.
კარბოქსილის მჟავები ურთიერთქმედებენ აქტიურ ლითონებთან, ლითონის ჰიდროქსიდებთან, მარილებთან:
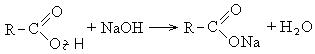
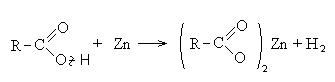
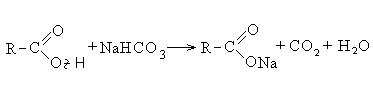
II რეაქციები C-OH ბმის გაწყვეტით (II მიმართულება).
C-OH ბმის დაშლის რეაქციები მიმდინარეობს ნუკლეოფილური ჩანაცვლების მექანიზმის (SN) მიხედვით და იწვევს კარბოქსილის მჟავების ე.წ. ფუნქციური წარმოებულების წარმოქმნას. Ესენი მოიცავს:
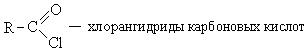
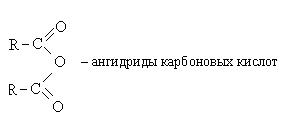
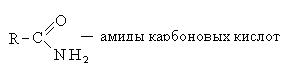

ნუკლეოფილური ჩანაცვლების რეაქციების მექანიზმი შემდეგია:
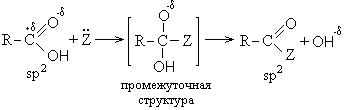
ნუკლეოფილი.
1. კარბოქსილის მჟავას ქლორიდების წარმოქმნა:
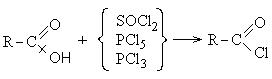

კარბოქსილის მჟავის ქლორიდები არის ნაერთების რეაქტიული კლასი და ფართოდ გამოიყენება ორგანულ სინთეზში დიოქსიკეტონებისა და კარბოქსილის მჟავების მისაღებად:
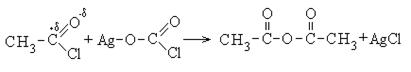
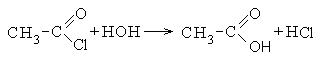
2. კარბოქსილის მჟავების ანჰიდრიდების წარმოქმნა:
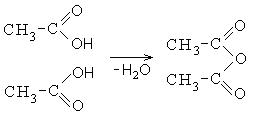
კარბოქსილის მჟავების ანჰიდრიდები ასევე რეაქტიული ნაერთებია. ძმარმჟავას ანჰიდრიდი გამოიყენება აცეტილირების აგენტად:
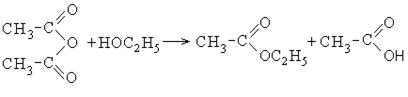
როდესაც ძმარმჟავას ანჰიდრიდი იხსნება წყალში, წარმოიქმნება ძმარმჟავა.
3. კარბოქსილის მჟავების ამიდების წარმოქმნა:
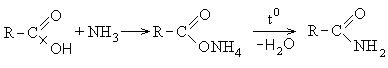
4. ეთერების წარმოქმნა:
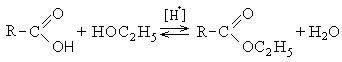
III. რეაქციები ნახშირწყალბადის რადიკალში (III მიმართულება). ეს რეაქციები მიმდინარეობს რადიკალური ჩანაცვლების მექანიზმით (S R):

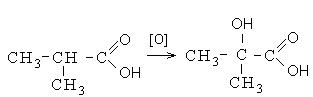
ურთიერთქმედების ზემოაღნიშნული მიმართულებების გარდა, კარბოქსილის მჟავები შედიან ჟანგვის რეაქციებში. კარბოქსილის მჟავების დაჟანგვა მიმდინარეობს მძიმე პირობებში ჰიდროქსი მჟავების წარმოქმნით. არაგანტოტვილ კარბოქსილის მჟავებში დაჟანგვა ხდება β-პოზიციაში, ხოლო განშტოებულ მჟავებში α-პოზიციაში კარბონილის ჯგუფის ნახშირბადის მიმართ:

კარბოქსილის მჟავების გამოყენება.ჭიანჭველა მჟავა- სითხე მძაფრი სუნით. მრეწველობაში ჭიანჭველა მჟავა მიიღება ნატრიუმის ფორმატისგან, რომელიც წარმოიქმნება ნახშირბადის მონოქსიდის გავლისას კაუსტიკური სოდას ხსნარში.

მიღებული მარილი თავისუფალ მჟავად გარდაიქმნება გოგირდმჟავას მოქმედებით:
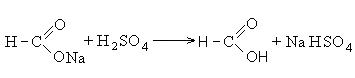
ჭიანჭველა მჟავა ფართოდ არის გავრცელებული ბუნებაში. გვხვდება ჭინჭარში, ნემსებში, ჭიანჭველების ნარჩენი პროდუქტია. ჭიანჭველა მჟავა გამოიყენება როგორც კონსერვანტი. მისი ხსნარი ეთანოლში ცნობილია როგორც ფორმული ალკოჰოლი.
ძმარმჟავა. ამ მჟავას ასევე უწოდებენ მყინვარულს, რადგან +16,5 0 C ტემპერატურაზე ის მყარდება კრისტალურ მასად. ძმარმჟავას აქვს დამახასიათებელი მძაფრი სუნი და შერწყმულია წყალთან ნებისმიერი თანაფარდობით. ძმარმჟავას 3-5%-იან ხსნარს უწოდებენ ძმარს, ხოლო 70-80%-იან ხსნარს. ძმრის ესენცია. საკვები მიზნებისთვის ძმარმჟავას წარმოქმნის ძმარმჟავას დუღილი.
მაღალი მოლეკულური წონის კარბოქსილის მჟავები(პალმიტური და სტეარიული). ამ მჟავების ნარევს სტეარინი ეწოდება. სტეარინი გამოიყენება სანთლების დასამზადებლად, ბაზის შესაქმნელად ტუჩსაცხებისთვის, ფეხსაცმლის კრემებისთვის. სტეარინი მიიღება ჰიდროლიზებული ცხიმის სუბლიმაციის შედეგად. სინთეზური სარეცხი საშუალებების აქტიური ბაზის მისაღებად გამოიყენება მაღალი მოლეკულური წონის კარბოქსილის მჟავები ნახშირბადის ატომების რაოდენობით C 10 -C 20.
ალკილის სულფატები ჩვეულებრივ გამოიყენება როგორც სარეცხი საშუალებების აქტიური ბაზა. ზოგადი სქემაალკილსულფონატების მიღება მცირდება შემდეგამდე:
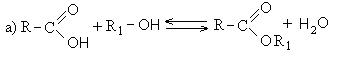
სარეცხი ეფექტი აქტიური ნივთიერებები. სურფაქტანტები არის ნაერთები, რომლებსაც შეუძლიათ ადსორბირება ინტერფეისზე და შეცვალონ მათი ზედაპირული დაძაბულობა. ზედაპირულად აქტიური ნივთიერებებისთვის სარეცხი თვისებები, ეხება:
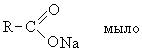
სურფაქტანტების სტრუქტურა შეიძლება ჩაითვალოს, როგორც ორი ფრაგმენტისგან შემდგარი: ჰიდროფილურინაწილი, ანუ წყალში ხსნადი და ჰიდროფობიურინაწილი, რომელიც წარმოდგენილია წყალში უხსნადი გრძელჯაჭვის ნახშირწყალბადის რადიკალით.
ზედაპირულად აქტიური ნივთიერებების სარეცხი ეფექტი აიხსნება შემდეგი ფაქტორებით: ზედაპირულად აქტიური ნივთიერებების ჰიდროლიზის დროს იქმნება ტუტე გარემო, რომელიც იწვევს ცხიმების ემულსიფიკაციას ზედაპირიდან. თავად სურფაქტანტები უზრუნველყოფენ ამ ემულსიების სტაბილურობას. სტაბილური ემულსიები წარმოიქმნება ცხიმის წვეთების ზედაპირზე ზედაპირულად აქტიური ნივთიერებების ადსორბციის გამო, რაც არ აძლევს ამ წვეთებს (ჭუჭყს) ერთმანეთთან შერწყმის საშუალებას და ჭუჭყი არ დევს ქსოვილზე, მაგრამ რჩება წყლის გარემოში და იხსნება. .
გაჯერებული (შემზღუდველი) კარბოქსილის მჟავები - ნაერთები (ნახშირწყალბადის რადიკალში არ არის მოკლე ბმები) აქვთ ზოგადი ფორმულა SlH2l + 1COOH. წარმოების მეთოდები 1. პირველადი სპირტების დაჟანგვა: 3CH3CH2OH + 2K2SG207 + 8H2S04 - 3CH3COOH + + 2K2S04 + 2Cr2 (S04)3 + 11H20 2. ალდეჰიდების დაჟანგვა: 5CH3CH2OH + 2K2SG207 + 8H2S04 - 3CH3COOH + + 2K2S04 + 2Cr2 (S04)3 + 11H20 2. ალდეჰიდების დაჟანგვა: 5CH3CH2OH H + R "-C00-R * + H20 ^ R "-COOH + R" OH კარბოქსილის მჟავას ჰალოიდები: არსებობს ცალკეული წარმომადგენლების მიღების სპეციფიკური მეთოდები (იხ. ჭიანჭველა და ძმარმჟავები). ფიზიკური თვისებები. ჰომოლოგიური სერიის პირველი წარმომადგენლები. ალკანური მჟავების (Q -C3) ნორმალურ პირობებში ადვილად მოძრავი სითხეებია მკვეთრი დამახასიათებელი სუნით. მაგალითად, ეთანოინის (ძმარმჟავას) აქვს დამახასიათებელი "ძმარვის" სუნი. ამ სერიის შუა წარმომადგენლები (C4 - Q) ბლანტია. , "ზეთოვანი" სითხეები დამახასიათებელი სუნით. მჟავები ათი ან მეტი ნახშირბადის ატომით მყარია. ნივთიერებები, რომლებიც პრაქტიკულად უსუნოა. კარბოქსილის მჟავები ძალიან ხსნადია ორგანულ გამხსნელებში; წყალში მათი ხსნადობა მცირდება ნახშირწყალბადის რადიკალის სიგრძის გაზრდით. 1-3 ნახშირბადის ატომის შემცველი მჟავები უსასრულოდ ერევა წყალთან, 4-9 - შეზღუდული, 10 და მეტი - პრაქტიკულად წყალში უხსნადი. კარბოქსილის მჟავების დუღილის წერტილი გაცილებით მაღალია, ვიდრე მათი შესაბამისი ალკოჰოლებისა და ალდეჰიდების დუღილის წერტილი. ეს აიხსნება იმით, რომ კარბოქსილის მჟავები აირისებრ მდგომარეობაში ქმნიან დიმერებს წყალბადის ბმების გამო, რომლებიც ადვილად წარმოიქმნება კარბოქსილის ჯგუფის სტრუქტურული მახასიათებლების გამო: O n-O R-C ^ ^ C-R. 29.2 მიუთითებს გაჯერებული კარბოქსილის მჟავების ზოგიერთი წარმომადგენლის ფიზიკურ თვისებებზე. ცხრილი 29.2. გაჯერებული კარბოქსილის მჟავების ზოგიერთი წარმომადგენლის ფუნქციური თვისებები მჟავის დასახელება ფორმულა დნობის წერტილი, °C დუღილის წერტილი, „C ფორმული HCOOH 8.2 100.5 ძმარმჟავა CHeCOOH 16.6 118.5 პრონიონური C2H5COOH -20.7 141.1 . |3COOH -10.5 223.0 Capric C7H15COOH 16D 237.5 Pelargonic CgHiTCOOH 12.5 253.0 Capric C9H19COOH 31.5 268.4 პალმიტური მჟავა C.5 H31COOH 62.6 3aCOOH 62.6 5COOH 271. კარბოქსილის მჟავები უფრო ძლიერი მჟავებია, ვიდრე სპირტები, ვინაიდან წყალბადის ატომმა კარბოქსილის ჯგუფში გაიზარდა მობილურობა CO ჯგუფის გავლენის გამო (იხ. ზემოთ). წყალხსნარში კარბოქსილის მჟავები იშლება: თუმცა, კარბოქსილის მჟავას მოლეკულების კოვალენტური ბუნების გამო, ზემოთ მითითებული დისოციაციის წონასწორობა საკმაოდ ძლიერად არის გადატანილი მარცხნივ. ამრიგად, კარბოქსილის მჟავები ზოგადად სუსტი მჟავებია. გაჯერებული მონობაზური კარბოქსილის მჟავების დისოციაციის მუდმივები მერყეობს 1.77-10"4 (HCOOH)-დან (QHnCOOH), ანუ ისეთ არაორგანულ მჟავებთან შედარებით, როგორიცაა HC1, HN03 ან H2S04, ისინი სუსტია, მაგრამ უფრო ძლიერი ვიდრე ნახშირმჟავა (Ki = 1). 10-7) 2. მარილების წარმოქმნა კარბოქსილის მჟავებს აქვთ ჩვეულებრივი მჟავების ყველა თვისება ისინი რეაგირებენ აქტიურ ლითონებთან, ძირითადი ოქსიდებისუსტი მჟავების ფუძეები და მარილები: კარბოქსილის მჟავები სუსტია, ამიტომ ძლიერი მინერალური მჟავები ანაცვლებენ მათ შესაბამისი მარილებისგან: CH3COONa + HCl -CH3COOH + NaCl წყალხსნარებში კარბოქსილის მჟავების მარილები ჰიდროლიზდება: CH3COOK + n20 CH3COOH + KOH განსხვავება კარბოქსილის მჟავები და მინერალური მჟავები მდგომარეობს რიგი ფუნქციური წარმოებულების წარმოქმნის შესაძლებლობაში. 3. კარბოქსილის მჟავების ფუნქციური წარმოებულების ფორმირება. კარბოქსილის მჟავებში OH ჯგუფის ჩანაცვლებისას სხვადასხვა ჯგუფები(X) წარმოიქმნება R-CO-X ზოგადი ფორმულის ფუნქციური მჟავა წარმოებულები; აქ R ნიშნავს ალკილის ან არილის ჯგუფს. მჟავა ქლორიდები მიიღება ფოსფორის (V) ქლორიდის მჟავებზე მოქმედებით: R-co-OH + pa5- * R-co-a + poa3 + Ha ეთერები წარმოიქმნება მჟავას სპირტით გახურებით გოგირდმჟავას თანდასწრებით. შექცევადი ესტერიფიკაციის რეაქცია): h2so4 ესტერიფიკაციის რეაქციის მექანიზმი დადგინდა „ტეგირებული ატომის“ მეთოდით. ეთერების მიღება შესაძლებელია აგრეთვე მჟავა ქლორიდების და ტუტე ლითონის ალკოჰოლატების რეაქციით: კარბოქსილის მჟავას ქლორიდების რეაქცია ამიაკთან იწვევს ამიდების წარმოქმნას: CH3 - CO - CI + 2NH3 - CH3 - CO - NH2 + NH4CI გარდა ამისა, ამიდების მიღება შესაძლებელია. კარბოქსილის მჟავების ამონიუმის მარილების გაცხელებით: t CH3-COONH4-»CH3-CO-NH2+H2O R-CO- 4. კარბოქსილის მჟავების მთელი რიგი თვისებები განპირობებულია ნახშირწყალბადის რადიკალის არსებობით. ამრიგად, სინათლეზე მჟავებზე ჰალოგენების მოქმედებით წარმოიქმნება ჰალოგენით შემცვლელი მჟავები და წყალბადის ატომი კარბოქსილის ჯგუფის მიმდებარე ნახშირბადის ატომში (ა-ატომი) იცვლება ჰალოგენით: 5. კარბოქსილის რედოქსული რეაქციები. მჟავები. 02 ატმოსფეროში ყველა კარბოქსილის მჟავა იჟანგება CO2-მდე და H20-მდე: CHeSCHUN + 202 -1 2CO2 + 2H2O გაჯერებული მონოკარბოქსილის მჟავები მდგრადია ისეთი ძლიერი ჟანგვის აგენტების მოქმედების მიმართ, როგორიცაა კონცენტრირებული HNO3 და H2SO4 (ფორმული მჟავის გარდა). . კარბოქსილის მჟავებს შემამცირებელი საშუალებების მოქმედებით კატალიზატორების არსებობისას შეუძლიათ ალდეჰიდებად ან სპირტებად გადაქცევა: 6. დეკარბოქსილირების რეაქციები. გაჯერებული შეუცვლელი მონოკარბოქსილის მჟავები მაღალი სიმტკიცის გამო C-C კავშირებიგაცხელებისას ისინი გაჭირვებით დეკარბოქსილირდება. ეს მოითხოვს კარბოქსილის მჟავას ტუტე ლითონის მარილის შერწყმას ტუტესთან: CH3-CH2-COONa + NaOH i CjHfij-f-Na2C03 ცალკეული წარმომადგენლები. ფორმული (მეთანის) მჟავა. სახელწოდება განპირობებულია იმით, რომ მჟავა შეიცავს ჭიანჭველების სეკრეციას. HCOOH არის უფერო სითხე მძაფრი სუნით. ჭიანჭველა მჟავა მიიღება ნახშირბადის მონოქსიდის (II) დაფხვნილი ნატრიუმის ჰიდროქსიდის გაცხელებით. სხვა გაჯერებული მონოკარბოქსილის მჟავებისგან განსხვავებით, ჭიანჭველა მჟავა არასტაბილურია კონცენტრირებული გოგირდის და აზოტის მჟავების მოქმედების მიმართ. ძლიერი შემცირების აგენტი: ტუტე ლითონის ფორმატები გარდაიქმნება ოქსილის მჟავას მარილებად. ძმარმჟავა CH3COOH არის უფერო სითხე მძაფრი სუნით. ძმარმჟავა მიიღება ბუტანის კატალიზური დაჟანგვით საკვები და ფარმაცევტული მიზნებისათვის ძმარმჟავა მიიღება ეთილის სპირტის შემცველი სითხეების ძმარმჟავას დუღილით. ძმარმჟავა ფართოდ გამოიყენება ქიმიურ, ფარმაცევტულ, კვების, ტექსტილისა და საღებავების მრეწველობაში. პალმიტური (ჰექსადეკანური) მჟავა ScH^COOH და სტეარინის (ოქტადეკანური) მჟავა C17H35COOH არის თეთრი მყარი, უსუნო და უგემოვნო, წყალში უხსნადი, ორგანულ გამხსნელებში ადვილად ხსნადი. ისინი უმრავლესობის ნაწილია მცენარეული ზეთებიდა ცხოველური ცხიმები. მიიღება ცხიმებისა და ზეთების საპონიფიკაციით. პალმიტისა და სტეარინის მჟავების ნარევს სტეარინი ეწოდება. მათი ქიმიური თვისებების მიხედვით ისინი არიან ტიპიური წარმომადგენლებიკარბოქსილის მჟავების შეზღუდვა. ფართოდ გამოიყენება სარეცხი საშუალებების წარმოებაში და კოსმეტიკაქიმიურ და ფარმაცევტულ მრეწველობაში.
მსგავსი სტატიები
-
ინგლისური - საათი, დრო
ყველას, ვისაც აინტერესებს ინგლისური ენის შესწავლა, მოუწია უცნაურ აღნიშვნებს გვ. მ. და ა. მ , და საერთოდ, სადაც დროა ნახსენები, რატომღაც მხოლოდ 12 საათიანი ფორმატი გამოიყენება. ალბათ ჩვენთვის მცხოვრები...
-
"ალქიმია ქაღალდზე": რეცეპტები
Doodle Alchemy ან Alchemy ქაღალდზე Android-ისთვის არის საინტერესო თავსატეხი ლამაზი გრაფიკით და ეფექტებით. ისწავლეთ როგორ ითამაშოთ ეს საოცარი თამაში და იპოვეთ ელემენტების კომბინაციები, რათა დაასრულოთ ალქიმია ქაღალდზე. Თამაში...
-
თამაშის ავარია Batman: Arkham City?
თუ თქვენ წინაშე აღმოჩნდებით, რომ Batman: Arkham City ანელებს, ავარია, Batman: Arkham City არ დაიწყება, Batman: Arkham City არ დაინსტალირდება, არ არის კონტროლი Batman: Arkham City, არ არის ხმა, გამოდის შეცდომები. ზევით, ბეტმენში:...
-
როგორ მოვიშოროთ ადამიანი სათამაშო აპარატებიდან როგორ მოვიშოროთ ადამიანი აზარტული თამაშებისგან
მოსკოვის Rehab Family კლინიკის ფსიქოთერაპევტთან და აზარტულ თამაშებზე დამოკიდებულების მკურნალობის სპეციალისტთან რომან გერასიმოვთან ერთად, რეიტინგის ბუკმეიკერებმა სპორტულ ფსონებში მოთამაშეს გზა გაუკვლიეს - დამოკიდებულების ჩამოყალიბებიდან ექიმთან ვიზიტამდე,...
-
Rebuses გასართობი თავსატეხები თავსატეხები გამოცანები
თამაში "RIDDLES Charades Rebuses": პასუხი განყოფილებაში "RIDDLES" დონე 1 და 2 ● არც თაგვი, არც ჩიტი - ის ხარობს ტყეში, ცხოვრობს ხეებზე და ღრღნის თხილს. ● სამი თვალი - სამი ბრძანება, წითელი - ყველაზე საშიში. დონე 3 და 4 ● ორი ანტენა თითო...
-
შხამისთვის თანხების მიღების პირობები
რამდენი თანხა მიდის SBERBANK-ის ბარათის ანგარიშზე გადახდის ოპერაციების მნიშვნელოვანი პარამეტრებია სახსრების დაკრედიტების პირობები და ტარიფები. ეს კრიტერიუმები, პირველ რიგში, დამოკიდებულია თარგმანის არჩეულ მეთოდზე. რა პირობებია ანგარიშებს შორის თანხის გადარიცხვისთვის
